
| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:C>A | |
| C. | 最高价氧化物对应水化物的酸性:D>C | |
| D. | 单质B常温下能溶于浓硝酸 |
分析 短周期主族元素A、B、C、D原子序数依次增大,B原子最外层电子数等于A原子最外层电子数的一半,则A原子最外层电子数为偶数,A、C的原子序数的差为8,则A、C为同主族元素,令B原子最外层电子数为x,则A、C的最外层电子数为2x,A、B、C三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解的x=3,故A、C的最外层电子数为6,A为O元素,C为S元素,B的原子序数大于氧元素,最外层电子数为3,故B为Al元素,D的原子序数最大,故D为Cl元素,据此解答.
解答 解:短周期主族元素A、B、C、D原子序数依次增大,B原子最外层电子数等于A原子最外层电子数的一半,则A原子最外层电子数为偶数,A、C的原子序数的差为8,则A、C为同主族元素,令B原子最外层电子数为x,则A、C的最外层电子数为2x,A、B、C三种元素原子的最外层电子数之和为15,则x+2x+2x=15,解的x=3,故A、C的最外层电子数为6,A为O元素,C为S元素,B的原子序数大于氧元素,最外层电子数为3,故B为Al元素,D的原子序数最大,故D为Cl元素.
A.同周期随原子序数增大原子半径减小,电子层越多原子半径越大,故原子半径O<Cl<S<Al,故A错误;
B.同主族自上而下非金属性减弱,故非金属性C<A,故B错误;
C.非金属性D(Cl)>C(S),故最高价氧化物对应水化物的酸性:D>C,故C正确;
D.常温下Al在浓硝酸中发生钝化现象,不能溶解,故D错误,
故选:C.
点评 本题考查结构位置性质关系,难度中等,关键是利用奇偶性及A、C的原子序数相差8判断二者处于同一主族(短周期),注意短周期中原子序数相差8不一定为同主族,如H与F.


科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 等浓度等体积的NaHSO3溶液与NaClO溶液混合后:c(Na++c(H+)═c(HSO3-)+c(ClO-)+2c(SO32-)+c(OH-) | |
| C. | 等浓度等体积的NaHCO3溶液与NaCl溶液混合后:$\frac{1}{2}$ c(Na+)═c(HCO3-)+c(CO32-)+c(H2CO3) | |
| D. | 标况下,将2.24LSO2气体通入到100ml 1mol•L-1的NaOH溶液中,完全反应后溶液呈酸性,则该溶液中: c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 血浆(7.35~7.45) | B. | 胰液(7.5~8.0) | C. | 胃液(0.9~1.5) | D. | 唾液(6.6~7.1) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH2N2)n | B. | C3H4ON5 | C. | C3H6N6 | D. | C4H4N5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A(g)的消耗速率与c(g)的生成速率比为2:3 | |
| B. | 由于该反应是等体积反应,所以增大压强正、逆反应速率不变 | |
| C. | 正、逆反应速率的比值是恒定的 | |
| D. | 当反应达到平衡状态时,充入一定量的A时,v正(A)增大的同时v逆(C)也增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大C或D的浓度 | B. | 减小B或A的浓度 | C. | 减小C或D的浓度 | D. | 充入稀有气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CN)2在碱溶液中生成CN-和OCN- | |
| B. | IBr+2NaOH═NaBr+NaIO+H2O | |
| C. | 均能在空气中燃烧 | |
| D. | IBr与苯发生取代反应生成溴苯和碘化氢 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
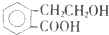 ,它可通过不同化学反应分别制得B、C、D、E四种物质.
,它可通过不同化学反应分别制得B、C、D、E四种物质.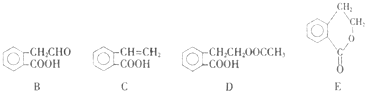
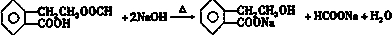 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com