
【题目】可以将反应Zn+Br2= ZnBr2设计成蓄电池,下列4个电极反应:
①Br2+ 2e-= 2Br- ②2Br-- 2e-= Br2③Zn – 2e-= Zn2+④Zn2++ 2e-= Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是
A.④和①B.②和①C.③和①D.②和③
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】下列内容与结论不对应的是
选项 | 内容 | 结论 |
A | H2O(g)变成H2O(l) | 该过程的ΔS<0 |
B | 硝酸铵溶于水可自发进行 | 因为ΔS>0 |
C | 一个反应的ΔH>0、ΔS>0 | 该反应一定不能自发进行 |
D | H2(g)+F2(g)=2HF(g) ΔH=-271 kJ·mol-1、 ΔS=8 J·mol-1·K-1 | 该反应在任何温度下均可自发进行 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下一系列反应,最终产物为草酸(乙二酸)。
B![]() C
C![]() D
D![]() E
E![]() F
F![]()
![]()
已知B为某一溴代物。
(1)推测用字母代表的化合物的结构式:C_______________。
(2)E→F的化学方程式是______________________。
(3)写出E和草酸在一定条件下生成高分子化合物的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知土壤胶体带负电,在土壤里施用含氮量相等的下列肥料,肥效较差的是( )
A.(NH4)2SO4
B.NH4HCO3
C.NH4NO3
D.NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列由事实得出的结论错误的是( )
A.维勒用无机物合成尿素,突破了无机物与有机物的界限
B.门捷列夫在前人工作的基础上总结出了元素周期律,表明科学研究既要继承又要创新
C.C60是英国和美国化学家共同发现的,体现了国际科技合作的重要性
D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究为主的学科
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R,X,Y,Z,A是短周期主族元素,它们在元素周期表中的相对位置如图所示.X原子最外层电子数等于电子层数的3倍.下列推断正确的是( ) 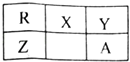
A.最简单气态氢化物的热稳定性由强到弱的排序:Z,R,X,Y
B.原子半径由小到大的排序:Z,A,Y,X
C.最高价氧化物的水化物酸性由弱到强的排Z,R,A
D.RY3 , A2X,ZA5分子中每个原子最外层都达到8 电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴及其化合物在生活和生产中都有重要应用,自然界中的溴绝大多数都分布在海洋中,从海水中提取溴是溴的最主要来源.
(1)海水中溴的主要存在形式是(填字母代号).
A.Br﹣
B.Br2
C.BrO﹣
D.BrO3﹣
(2)实验室若要直接浓缩海水时,下列仪器肯定不需要的是 . 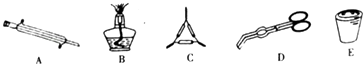
(3)工业上常将海水中的溴转化为单质,再用热空气吹出溴,采用以下两种方式吸收:
方法I、二氧化硫水溶液吸收,该方法中二氧化硫是(填“氧化剂”或“还原剂”).
方法II、纯碱溶液吸收法,生成物之一是NaBrO3 , 写出反应的化学方程式 .
(4)现有一份吸收了溴的无色溶液X,假定吸收剂和溴完全反应,通过下列实验可探究X是采用哪种方法吸收溴的(已知pH试纸遇酸变红,遇碱变蓝).
①用玻璃棒蘸取少量X点在pH试纸上,试纸呈色,证明X是采用方法I吸收的;另取少量X,依次加入稀硫酸和四氯化碳,充分振荡后静置,观察到溶液分层,(填“上”或“下”)层呈橙红色,有关反应的离子方程式为 , 证明X是采用方法II吸收的.
②请再设计一个实验验证X是采用方法I吸收溴所得的溶液 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是氧族部分元素的相关性质。
元素 性质 | 8O | 16S | 34Se | 52Te |
主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
原子半径 | 逐渐增大 | |||
单质与H2 反应情况 | 点燃时 易化合 | 加热 化合 | 加热 难化合 | 不能 直接化合 |
请回答下列问题:
(1)硒在周期表中位置____。
(2)碲的化合价可能有____。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是__________(填化学式)。
(4)氢硒酸有较强的____(填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_____________。
(5)氧族元素单质与H2反应过程中的焓变如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表___,d代表___(均写单质名称)。
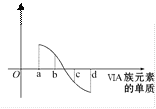
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以玉米淀粉为原料生产燃料乙醇的生产过程可由下图表示:
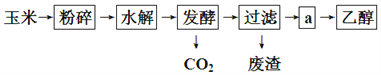
(1)乙醇分子中所含的官能团的名称为:__________________;
(2)过滤后得到a的主要成分为葡萄糖和乙醇,步骤a的操作是__________;
A.蒸发 B.萃取 C.蒸馏 D.分液
(3)生产过程中为了检验水解是否开始,可使用的试剂是______________;
(4)已知1g乙醇完全燃烧放出的热量为29.7kJ,请据此写出乙醇燃烧的热化学方程式:_______。
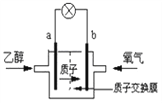
(5)为了充分利用乙醇的能量,科学家还把乙醇设计成燃料电池,如图,用磺酸类质子溶剂,在高温供电时,乙醇电池效率高且更安全。请判断,该电池的a极为电池的_______极(填“正”或“负”),b极的电极反应式为:____________________________,电池工作时,若有1mol乙醇被氧化,则转移的电子为____________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com