
吸食或注射毒品会危及人体健康,下列各组中的物质都属于毒品的是
A.冰毒、青霉素 B.海洛因、冰毒
C.尼古丁、碘盐 D.大麻、摇头丸
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+
B.加入K3[Fe(CN)6]溶液,产生特征蓝色沉淀,则原溶液一定有Fe3+
C.加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO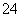
D.加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH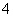
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气、溴蒸气分别与氢气反应的热化学方程式如下:
H2(g)+Cl2(g)===2HCl(g) ΔH1=-Q1kJ/mol
H2(g)+Br2(g)===2HBr(g) ΔH2=-Q2kJ/mol
已知Q1>Q2>0。
下列说法正确的是
A.上述两个反应中反应物的总能量均大于生成物的总能量
B.上述两个反应中反应物的总能量均小于生成物的总能量
C.H2(g)和Cl2(g)反应生成1 mol HCl(g)时放出Q1kJ的热量
D.1molHBr(g)具有的能量大于1molHBr(l)具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组欲测定某品牌味精中氯化钠的含量。该小组的实验步骤如下:
①称取该味精样品10.0g放入烧杯中,并加适量蒸馏水完全溶解;
②加入过量的用硝酸酸化的硝酸银溶液(假定只有NaCl与AgNO3溶液反应)。
③过滤;
④用蒸馏水洗涤沉淀2~3次;
⑤将沉淀烘干、称量,测得其质量为5.74g;
请回答下列问题:
(1)上述实验步骤③操作中所用到的玻璃仪器有 。
(2)若此品牌味精包装袋上标注:“谷氨酸钠含量≥80.0% ,氯化钠含量≤20.0%”;(假设样品中不含其它杂质)。通过上述实验结果,可计算出样品中氯化钠的质量分数为 ,所以该样品 (填“合格”或“不合格”)。
(3)检验上述实验步骤④所得沉淀是否洗净的方法是:取最后一次洗涤液少量,
。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室保存下列试剂的方法不正确的是
A.NaOH溶液存放在带橡胶塞的细口玻璃瓶中
B.氯水存放在棕色细口玻璃瓶中,并置于冷暗处
C.浓硫酸存放在带橡胶塞的细口玻璃瓶中
D.金属钠用煤油液封于广口玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列氧化还原反应在溶液中均能发生。
①2Fe3++2I-=2Fe2++I2;②2Fe2++Br2=2Fe3++2Br-;③2Br-+Cl2=2Cl-+Br2。
(1)Fe2+、Br-、I-三种微粒按还原性由强到弱的顺序为____________________。
(2)现有某混合溶液中含a mol FeI2和b mol FeBr2,向该混合液中逐渐通入c mol Cl2,试根据以上化学原理分析,当只有I-被氧化时,c的取值范围是______________。
(3)某混合溶液中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4。向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余Fe2+的物质的量之比为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化石燃料开采、加工过程产生的H2S 废气制取氢气,既价廉又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气。
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质子数之和为27,则R的原子结构示意图为________。
②常温下,不能与M单质发生反应的是____________(填序号)。
a.CuSO4溶液 b.Fe2O3 c.浓硫酸
d.NaOH溶液 e.Na2CO3固体
(2)利用H2S废气制取氢气的方法有多种。
①高温热分解法
已知:H2S(g)  H2(g)+
H2(g)+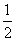 S2(g)
S2(g)
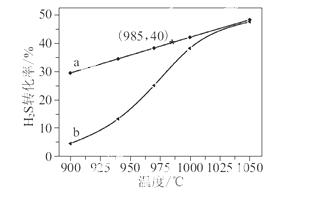
在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见图所示。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算 985 ℃时H2S按上述反应分解的平衡常数K=________;说明随温度的升高,曲线b向曲线a逼近的原因:_______________________________。
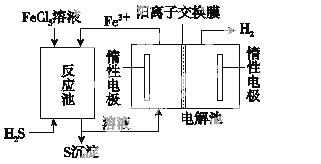
②电化学法
该法制氢过程的示意图如图所示。反应池中反应物的流向采用气、液逆流方式,其目的是
________________________________________________________________________;
反应池中发生反应的化学方程式为_____________________________________________
________________________________________________________________________。
反应后的溶液进入电解池,电解总反应的离子方程式为__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com