
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
有一包白色固体,它可能是KCl、K2CO3、KNO3中的一种或几种,进行下列实验:
①溶于水,得无色溶液;
②在所得溶液中滴入AgNO3溶液,生成白色沉淀(说明:Ag2CO3为白色沉淀);
③再滴加稀硝酸,沉淀量减少但不完全消失,同时有气泡生成。
根据上述现象判断:
(1)白色固体一定含有的成分是________,可能含有的成分是________。
(2)请写出上述实验中有关反应的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为配制250 mL 0.2 mol/L Na2CO3溶液的示意图。
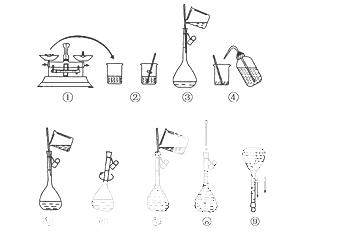
回答下列问题:
(1)①中称得Na2CO3________g;选取容量瓶规格:______________
(2)容量瓶使用前检验漏水的方法是 ____________________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.某同学在第⑧步观察液面时俯视________;
B.没有进行操作步骤④和⑤________;
C.在第⑤步不慎有少量液体流到容量瓶外 ________。
D 未经冷却趁热将溶液注入容量瓶中定容 ________。
E摇匀后发现液面低于刻度线再加水 _______
查看答案和解析>>
科目:高中化学 来源: 题型:
组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了如图所示的装置。
(1)检查图所示装置气密性的方法是________________________________________________。
(2)分别写出Al和Fe与硫酸反应的离子方程式
_____________________________ , _______________________。
(3)若要比较产生气体的快慢,可以测量相同时内产生气体的体积,也可以测量________________________________________。
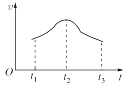 (4)实验测得铝丝产生气体的速率(v)与时间(t)的关系如图所示,分析不同时间段速率变化的原因:
(4)实验测得铝丝产生气体的速率(v)与时间(t)的关系如图所示,分析不同时间段速率变化的原因:
t1─t2 阶段速率加快的原因________________________。
t2─t3 阶段速率减慢的原因_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.5L的Fe2(SO4)3溶液中Fe3+的浓度为0.2mol/L,与0.2L0.5mol/L的Na2SO4溶液中SO42-的浓度之比是( )
A.3:2 B.2:5 C.3:5 D.5:3
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法中,正确的是 ( )
A.2.4 g金属镁所含电子数目为0.2 NA
B.16 g CH4所含原子数目为NA
C.17 g NH3 所含氢原子数目为4 NA
D.18 g水所含分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中有100 g氧气和足量的过氧化钠,向其中充入5 g CO和H2的混合气体后,用电火花点燃,反应足够长时间后,容器内气体的质量为( )。
A.大于100 g B.小于100 g C.等于100 g D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com