
| A. | $\frac{3}{8}$ mol | B. | $\frac{8}{3}$ mol | C. | $\frac{2}{3}$ mol | D. | $\frac{3}{2}$ mol |
分析 铜和稀硝酸发生3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,如是很稀的硝酸,可能发生4Cu+10HNO3(稀)=4Cu(NO3)2 +NH4NO3+5H2O,结合反应的方程式计算该题.
解答 解:铜和稀硝酸发生3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,被还原的硝酸等于生成NO的物质的量,
则3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O
3 2
n 1mol
n=$\frac{3}{2}$mol,
如是很稀的硝酸,可能发生4Cu+10HNO3(稀)=4Cu(NO3)2 +NH4NO3+5H2O,如果有1mol的硝酸被还原,则被氧化的铜的物质的量为0.25mol,
只有D符合,
故选D.
点评 本题考查硝酸的性质,侧重于学生的分析能力和计算能力的考查,为高频考点,注意根据反应的方程式进行判断,难度不大,


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-十H2O═2HCO3- | |
| B. | 少量小苏打溶液滴入Ba(OH)2溶液中:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 硫氢化钠发生水解:HS-+H2O?H3O++S2- | |
| D. | 氧化亚铁加入稀硝酸:FeO+2H+═Fe2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
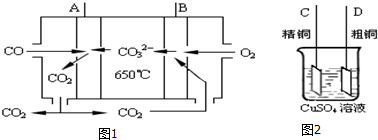
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
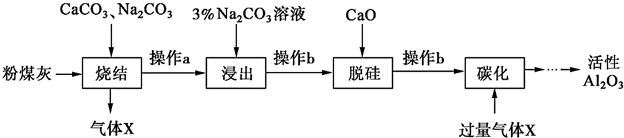
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
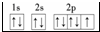 ;E3+的离子符号为Fe3+.
;E3+的离子符号为Fe3+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某微粒空间构型为三角锥形,则该微粒一定是极性分子 | |
| B. | 某微粒空间构型为V形,则中心原子一定有孤电子对 | |
| C. | NH4+中N-H键能、键长和键角均相同 | |
| D. | SiF4和SO${\;}_{3}^{2-}$的中心原子均为sp3杂化,其立体构型都是正四面体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com