
两种无机盐A和B,式量都为120.为确定A和B,进行如下验:①取少许A和B分别溶于水制成溶液;②取适量两种溶液混合加热,有无色刺激性气味的气体产生;③取适量两种溶液分别加入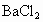 溶液,A溶液无明显现象,B溶液有白色沉淀生成;④取适量两种溶液分别加入
溶液,A溶液无明显现象,B溶液有白色沉淀生成;④取适量两种溶液分别加入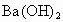 溶液,均有白色沉淀析出.
溶液,均有白色沉淀析出.
(1)推断A、B两种物质的化学式:A_________,B________.
(2)写出②④两步实验的离子方程式:
②步__________________________________________________.
④步__________________________________________________.
|
(1) 
(2) ②
将定性实验和定量计算结合推断.一般方法先根据实验现象,先假设几种具有这些性质的可能物质类别,进而筛选完全符合定性实验可能的物质,再利用式量确定物质,写出化学式,最检验是否完全符合题意.这是在发散思维基础上的收敛思维. 根据实验中产生气体的气味、颜色,可初步认为是 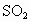 .两种盐中必有一种是硫酸氢盐,在此起酸的作用,提供 .两种盐中必有一种是硫酸氢盐,在此起酸的作用,提供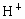 ;另一种盐可能是亚硫酸盐或者是亚硫酸氢盐.根据实验③的现象, ;另一种盐可能是亚硫酸盐或者是亚硫酸氢盐.根据实验③的现象,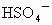 在水溶液中可以 在水溶液中可以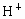 和 和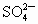 的形式存在,跟 的形式存在,跟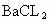 溶液生成 溶液生成 白色沉淀,另一种盐A则不与 白色沉淀,另一种盐A则不与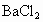 生成沉淀,说明A不是亚硫盐,只能是亚硫酸氢盐,则B为硫酸氢盐.根据实验④加入 生成沉淀,说明A不是亚硫盐,只能是亚硫酸氢盐,则B为硫酸氢盐.根据实验④加入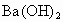 溶液,A中 溶液,A中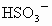 与之反应生成 与之反应生成 和 和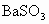 沉淀,定性实验表示A为亚硫酸氢盐,B为硫酸氢盐. 沉淀,定性实验表示A为亚硫酸氢盐,B为硫酸氢盐.
两种盐的式量均为 120,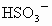 的式量为81,而 的式量为81,而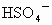 的式量为97,可确定A中存在阳离子的式量为120-81=39,恰好等于钾的相对原子质量,以A中含有钾离子,A为 的式量为97,可确定A中存在阳离子的式量为120-81=39,恰好等于钾的相对原子质量,以A中含有钾离子,A为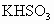 ;B中阳离子的式量为120-97=23,恰好等于钠元素的相对原子质量,所以B中含有 ;B中阳离子的式量为120-97=23,恰好等于钠元素的相对原子质量,所以B中含有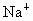 ,B为 ,B为 . . |


科目:高中化学 来源:物理教研室 题型:058
两种无机盐A和B,式量都为120.为确定A和B,进行如下验:①取少许A和B分别溶于水制成溶液;②取适量两种溶液混合加热,有无色刺激性气味的气体产生;③取适量两种溶液分别加入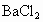 溶液,A溶液无明显现象,B溶液有白色沉淀生成;④取适量两种溶液分别加入
溶液,A溶液无明显现象,B溶液有白色沉淀生成;④取适量两种溶液分别加入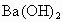 溶液,均有白色沉淀析出.
溶液,均有白色沉淀析出.
(1)推断A、B两种物质的化学式:A_________,B________.
(2)写出②④两步实验的离子方程式:
②步__________________________________________________.
④步__________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两元素原子最外电子层上电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A和C可以形成化合物CA3;B与D的原子序数之比为3︰4;E原子最外层电子数比次外层电子数少1。请回答:
(1)E在元素周期表的位置为:_▲_
(2)A、B、C、D原子半径从大到小的顺序为:_▲_(填元素符号)
(3)由A、B两种元素组成的分子有多种,其中一种分子含4个原子,且分子为直线型的对称结构,写出其电子式_▲_。
(4)甲由A、B、C、D四种元素组成的无机盐,既可以与盐酸反应又可以与NaOH溶液反应,其化学式为_▲_。
(5)由A、C、E三种元素组成的化合物C2A6E2是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出该化合物第一步水解反应的离子方程式_▲_。
(6)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程简单表示如下:
①将化合物CA3通入等物质的量混合的FeSO4、Fe2(SO4)3溶液中,生成两种碱,写出该过程的总离子方程式_▲_。
②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为_▲_。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍, A与D可以形成原子个数比分别为1:1和2:1的两种液态化合物;E单质用于净化水质。
请回答:
(1)写出D在元素周期表中的位置 ,E的原子结构示意图是_____,
下列可以验证C与D两元素原子得电子能力强弱的实验事实是__________(填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)由A、B两种元素组成的最简单的化合物,写出其电子式 。
(3)均由A、B、C、D四种元素组成的甲、乙两种化合物,都既可以与盐酸反应又可以与NaOH溶液反应,甲为无机盐,其化学式为 ,乙为天然高分子化合物的水解产物,且是同类物质中相对分子质量最小的,其结构简式为 。
(4)由A、C、E三种元素组成的化合物C2A6E2是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出该化合物第一步水解的离子反应方程式 ____________________。
(5)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该过程的总离子方程式____ 。
②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2011届浙江省苍南中学高三上学期期中考试化学试卷 题型:填空题
(13分)短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两元素原子最外电子层上电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A和C可以形成化合物CA3;B与D的原子序数之比为3︰4;E原子最外层电子数比次外层电子数少1。请回答:
(1)E在元素周期表的位置为:_▲_
(2)A、B、C、D原子半径从大到小的顺序为:_▲_(填元素符号)
(3)由A、B两种元素组成的分子有多种,其中一种分子含4个原子,且分子为直线型的对称结构,写出其电子式_▲_。
(4)甲由A、B、C、D四种元素组成的无机盐,既可以与盐酸反应又可以与NaOH溶 液反应,其化学式为_▲_。
液反应,其化学式为_▲_。
(5)由A、C、E三种元素组成的化合物C2A6E2是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出该化合物第一步水解反应的离子方程式_▲_。
(6)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程简单表示如下:
①将化合物CA3通入等物质的量混合的FeSO4、Fe2(SO4)3溶液中,生成两种碱,写出该过程的总离子方程式_▲_。
②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为_▲_。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com