
| A. | 1molNa被完全氧化生成Na2O2时失去2mole- | |
| B. | Na2O2常用作呼吸面具的供氧剂,使用过程中涉及氧化还原反应 | |
| C. | 热稳定性:NaHCO3>Na2CO3 | |
| D. | 纯碱是面包发酵粉和碱性洗涤剂的主要成分之一 |
分析 A.反应后钠元素变为+1价;
B.Na2O2中O元素化合价为-1价,反应后分别变为0价、-2价;
C.碳酸氢钠不稳定,加热易分解;
D.面包发酵粉的主要成分是碳酸氢钠.
解答 解:A.由于反应后钠元素变为+1价,故1mol钠失去1mol电子,故A错误;
B.Na2O2中O元素化合价为-1价,反应后分别变为0价、-2价,元素化合价发生变化,属于氧化还原反应,故B正确;
C.碳酸氢钠不稳定,加热分解生成碳酸钠,可知碳酸钠较稳定,故C错误;
D.面包发酵粉的主要成分是碳酸氢钠,易分解生成二氧化碳气体,易与酸反应,故D错误.
故选B.
点评 本题考查较为综合,涉及元素化合物的综合应用,为高频考点,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 |
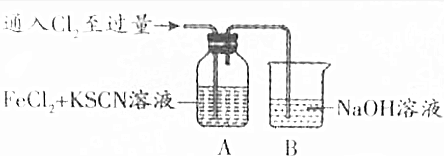 | Ⅰ.装置A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
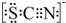
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3 | B. | AlCl3 | C. | HCl | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
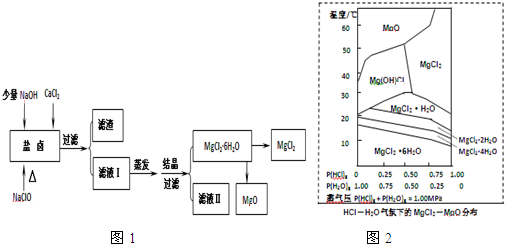
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
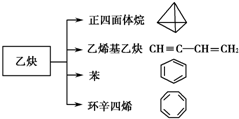 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物. .
. 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com