
在实验室用下图装置制取溴苯,回答:
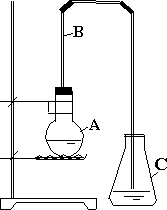
(1)烧瓶A中装有________、________和铁粉,铁粉在反应中是__________________.
(2)未加入铁粉时溴溶于苯不反应,当加入铁粉后观察到A中反应混合物逐渐沸腾,B管中有红棕色的蒸气.C出口附近有白雾.导管B起________和________的作用.导管C不插入水中是因为________________.
(3)反应完毕,向锥形瓶中滴入AgNO3溶液,有________生成;烧瓶A中的液体倒入盛水烧杯中烧杯底部有褐色不溶于水的油状物生成.
(4)纯净的溴苯无色液体,密度大于水.不纯的则显褐色,是由于其中________,可将其用________溶液通过洗涤、________来提纯.
(5)完成该反应的化学方程式:
_________________________________________________.
科目:高中化学 来源:高中化学同步单元练习册 全册 高二年级 题型:058
电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而可测定电石中碳化钙的质量分数.
实验室用下图装置进行测定电石中碳化钙质量分数的实验.

(1)如果所制气体流向为从左→右时,装置A、B、C的排列顺序是________,导管口连接顺序是________.
(2)仪器连接好后,进行实验时有下列操作(每项操作只进行一次):
①称取一定量电石,置于装置C中,塞紧橡胶塞;
②检查装置的气密性;
③在装置A和C的分液漏斗中注入适量的水;
④待装置C恢复到室温时,测量装置B中水的体积(导管中存有的水忽略不计);
⑤慢慢开启装置C的分液漏斗的活塞,使水逐滴滴下,至不产生气体时关闭活塞.
正确操作顺序(填写编号)是________.
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为气体中含有________杂质.
(4)若实验时称取的电石为1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数为________.
查看答案和解析>>
科目:高中化学 来源:2007年无锡市秋学期高三期末调研试卷化学-旧人教 题型:058
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广西南宁九中高二上学期段考理科化学试卷(带解析) 题型:实验题
某课外活动小组在实验室用下图的一些装置组合后,快速制取氨并验证氨的某些性质,同时收集少量纯净氮气,请回答: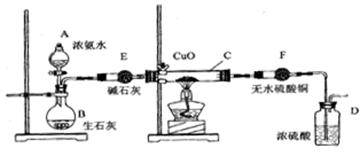
(1)写出用熟石灰和氯化铵反应制氨气的化学方程式
(2) 本实验进行一断时间后,观察到加热的硬质玻璃试管内黑色氧化铜粉末转为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃试管内发生反应的化学方程式: ,这个反应说明氨气具有____(填编号:A、碱性;B、还原性;C、氧化性; D、不稳定性)
(3) 洗气瓶中盛浓硫酸的主要作用是__________________
(4) 在最后的出气的导管口收集干燥、纯净的氮气,收集方法是:___________
(填编号:A、排气法 B、排水法 C、用气囊收集)
(5)装置E的作用是_______________。装置F验证的气体是___________。
查看答案和解析>>
科目:高中化学 来源:2014届广西南宁九中高二上学期段考理科化学试卷(解析版) 题型:实验题
某课外活动小组在实验室用下图的一些装置组合后,快速制取氨并验证氨的某些性质,同时收集少量纯净氮气,请回答:
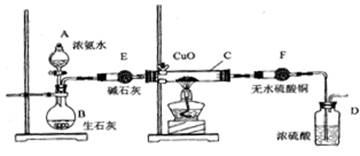
(1)写出用熟石灰和氯化铵反应制氨气的化学方程式
(2) 本实验进行一断时间后,观察到加热的硬质玻璃试管内黑色氧化铜粉末转为红色,盛无水硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃试管内发生反应的化学方程式: ,这个反应说明氨气具有____(填编号:A、碱性 ;B、还原性;C、氧化性; D、不稳定性)
(3) 洗气瓶中盛浓硫酸的主要作用是__________________
(4) 在最后的出气的导管口收集干燥、纯净的氮气,收集方法是:___________
(填编号:A、排气法 B、排水法 C、用气囊收集)
(5)装置E的作用是_______________。装置F验证的气体是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引 起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
已知:CO2、碳酸盐、碳酸氢盐的部分性质如下:
CO2(过量)+OH一=HCO3- HCO3-+OH一=CO32一+H2O
CO32-+H+反应生成CO2分两步:
第一步:CO32-+H+= HCO3- 第二步:HCO3- +H+=CO2↑+ H2O
(1)目前,用超临界CO2( 其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对保护环境的作用是 。
(2)最近有科学家提出“绿色自由’’构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,在一定条件下与H2反应,使之变为可再生燃料甲醇。其流程如下:

①写出CO2与H2反应制得甲醇的化学方程式: 。
②某同学在实验室用下图所示的装置和药品制取K2 CO3溶液,他所制得的溶液中可能含有的杂质是
。

③某同学在数字化实验室中用传感器对碳酸钾和碳酸氢钾的混合物样品进行成分测定,他分别称取三份不同质量的混合物样品,配成溶液,然后逐滴加人相同浓度的稀硫酸,测得如下数据:

则该混合固体中K2CO3与KHCO3的物质的量之比是 ;所用硫酸的物质的量浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com