
 钢铁易生锈是因为在潮湿的空气里,其表面吸附一层薄薄的水膜,构成了若干微小原电池(如图所示).下列有关说法正确的是( )
钢铁易生锈是因为在潮湿的空气里,其表面吸附一层薄薄的水膜,构成了若干微小原电池(如图所示).下列有关说法正确的是( )| A. | O2在正极参加反应,生成OH- | |
| B. | 钢铁生锈过程中电能转化为化学能 | |
| C. | 负极的电极反应式为:Fe-3e -=Fe3+ | |
| D. | 为减缓铁制品生锈,可将其与铜相连 |
分析 A.钢铁在潮湿空气里发生电化学腐蚀时,铁做负极,发生氧化反应,氧气做正极发生还原反应;
B.钢铁易生锈是因为在潮湿的空气里,其表面吸附一层薄薄的水膜,构成了若干微小原电池;
C.上述电化学腐蚀中,铁失电子发生氧化反应,做负极失电子生成亚铁离子;
D.钢铁与铜相连,在电解质溶液中形成原电池反应,钢铁做负极被腐蚀.
解答 解:A.在中性环境中,氧气得电子生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-,故A正确;
B.钢铁易生锈是因为在潮湿的空气里,其表面吸附一层薄薄的水膜,构成了若干微小原电池,钢铁生锈过程中化学能转化为电能,故B错误;
C.负极的电极反应式为:Fe-3e -=Fe2+,故C错误;
D.与铜相连电解质溶液中形成原电池反应钢铁做负极被腐蚀,不能减缓铁制品生锈,故D错误;
故选A.
点评 本题考查金属腐蚀与防护,明确原电池原理即可解答,知道钢铁发生析氢腐蚀和吸氧腐蚀的区别,知道防止金属腐蚀的方法,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有x+2 | B. | 可能是x+2 或x+10或x+24 | ||
| C. | 可能是x+24 | D. | 可能是x+2或x+12或x+26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃,5 mL 3% H2O2溶液 | |
| B. | 10℃,5 mL 5% H2O2溶液 | |
| C. | 30℃,5 mL 5% H2O2溶液 | |
| D. | 30℃,5 mL 5% H2O2溶液且加入少量MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的结构简式:C6H6 | B. | 二氧化碳的电子式: | ||
| C. | KNO3电离方程式:KNO3=K++NO3- | D. | Cl-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+具有氧化性,可溶解印刷电路板上的金属铜 | |
| B. | 碳酸钡、硫酸钡均难溶于水,均可用作钡餐 | |
| C. | 氧化铝具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | 二氧化硅具有半导体性能,可以制成光电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,20 g D2O分子中所含中子数为10 NA | |
| B. | 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA | |
| C. | 将lmol Cl2通入水中,HC1O、Cl-、C1O-粒子数之和为2 NA | |
| D. | 常温常压下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
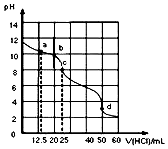 常温下,用0.1000mol•L-1盐酸滴定25mL0.1000mol•L-1Na2CO3溶液,其滴定曲线如图所示,对滴定过程中所得溶液相关离子浓度间的关系,下列有关说法正确的是( )
常温下,用0.1000mol•L-1盐酸滴定25mL0.1000mol•L-1Na2CO3溶液,其滴定曲线如图所示,对滴定过程中所得溶液相关离子浓度间的关系,下列有关说法正确的是( )| A. | a点:c(Cl-)>c(HCO3-)>c(CO32-) | |
| B. | b点:c(Na+)+c(H+)=c(Cl-)+c(HCO3-)+c(CO32-)+c(OH-) | |
| C. | c点:c(CO32-)+c(OH-)=c(H+)+c(H2CO3) | |
| D. | d点:c(Na+)=0.1000mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 向该装置中加入金属Zn和稀硫酸,并关闭活塞,用于检查装置的气密性 | 用该装置制备少量白色的Fe (OH)2沉淀 | 灼烧CuSO4使其分解 | 分离葡萄糖和蔗糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com