
| A.钠露置在空气中表面生成淡黄色的Na2O |
| B.将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| C.将CO2通入次氯酸钙溶液可生成次氯酸 |
| D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 在Ba(NO3)2溶液中分别滴入H2SO3及H2SO4溶液 | 均有白色沉淀 | 沉淀均为BaSO4 |
| B | 混合装有Cl2和NH3量集气瓶中的气体 | 产生大量白烟 | NH3显还原性和碱性 |
| C | 溶液X中滴入盐酸酸化的FeCl2溶液,再滴入淀粉溶液 | 溶液变蓝色 | 溶液X中一定含有I- |
| D | 向浓度居委0.01mol/LNaCl和Na2S的混合溶液中滴入少量AgNO3 | 出现黑色沉淀 | Ksp(Ag2S)>Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | ⑦ | | | | | | | | | | | | | | | ⑧ | |
| | | | | | | | ⑨ | | | ⑩ | | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Ca(ClO)2溶液暴露于空气中,一段时间后其pH变小 |
| B.向一定体积的热浓硫酸中加入足量的铁粉,生成的气体能被烧碱溶液完全吸收 |
| C.第ⅥA族元素的氢化物中,稳定性最强的其沸点最高 |
| D.共价键、离子键、范德华力和氢键是形成晶体的四种作用力,这四种力不可能同时存在于同一晶体中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④ | B.①④ | C.①③④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部都是 | B.①②⑤⑧⑩ |
| C.①②⑤⑦⑧⑩ | D.①②④⑤⑦⑧⑨⑩ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
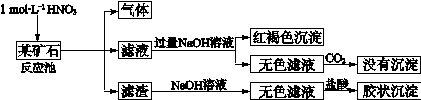
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2的水溶液能导电说明SO2是电解质 |
| B.HClO是弱酸,所以NaClO是弱电解质 |
| C.某无色溶液加入NaOH溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则该溶液含有NH4+ |
| D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液一定存在大量CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com