
(07年广东卷)(10分)已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45~50%),另一个产物A也呈酸性,反应方程式如下:
C6H5CHO+(CH3CO)2O → C6H5CH=CHCOOH+ A
苯甲醛 肉桂酸
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为11。产物A的名称是
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为________(不要求标出反应条件)
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
取代苯甲醛 |
|
|
|
|
产率(%) | 15 | 23 | 33 | 0 |
取代苯甲醛 |
|
|
|
|
产率(%) | 71 | 63 | 52 | 82 |
可见,取代基对Perkin反应的影响有(写出3条即可):
①
②
③
(4)溴苯(C6H5Br)与丙烯酸乙酯(CH2=CHCOOC2H5)在氯化钯催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为_________(不要求标出反应条件)
(5)Beck反应中,为了促进反应的进行,通常可加入一种显 (填字母)的物质
A 弱酸性 B 弱碱性 C 中性 D 强酸性
答案:(1)乙酸
(2)C6H5CH=CHCOOH+C2H5OH → C6H5CH=CHCOOC2H5+H2O
(3)①苯环上有氯原子取代对反应有利
②苯环上有甲基对反应不利
③氯原子离醛基越远,对反应越不利(或氯原子取代时,邻位最有利,对位最不利)
④甲基离醛基越远,对反应越有利(或甲基取代时,邻位最不利,对位最有利)
⑤苯环上氯原子越多,对反应越有利
⑥苯环上甲基越多,对反应越不利
(4)C6H5Br+CH2=CHCOOC2H5→C6H5CH=CHCOOC2H5+HBr
(5)B
解析:难度中等,本题反映原理较新,相信参加过化学竞赛的同学会觉得更易入手一些,题目中的方程式可以利用原子守恒及已学原理搞定,官能团对反应活性的影响也不难观察出,解题时可从官能团种类、官能远近,官能团多少来分析其对产率的影响。考查学生对有机化合物分子式与命名、组成和结构特点及其相互联系的了解,以及对酯化反应、取代反应等的了解,考查学生通过推理获取新知识和归纳与文字表达能力、信息迁移能力双及以上各部分知识的综合运用能力。此类题应该说在一定意义上是05、06年有机题的翻版,但信息不同又有创新,很好地考查学生摄取信息,分析信息总结归纳能力。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
(07年广东卷)灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
① Sn(s、白) + 2HCl(aq)= SnCl2(aq)+ H2(g) △H1
② Sn(s、灰) + 2HCl(aq)= SnCl2(aq)+ H2(g) △H2
③ Sn(s、灰)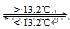 Sn(s、白) △H3= + 2.1kJ/mol
Sn(s、白) △H3= + 2.1kJ/mol
下列说法正确的是( )
A. △H1 >△H2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
(07年广东卷)(11分)已知某混合金属粉末,除铝处还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1:该混合金属粉末中除铝外还含有 元素;
假设2:该混合金属粉末中除铝外还含有 元素;
假设3:该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超过答题卡空间。

查看答案和解析>>
科目:高中化学 来源: 题型:
(07年广东卷)(10分)C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为_____________
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是_________
(3)按要求指出下列氧化物的空间构型、成键方式或性质_________
①CO2分子的空间构型及碳氧之间的成键方式 ______________ ;
②SiO2晶体的空间构型及硅氧之间的成键方式 ______________ ;
③已知SnO2是离子晶体,写出其主要物理性质__________ (写出2条即可)
CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为 ________________
(4)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度________ (填字母)
A 强 B 弱 C 相等 D 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
(07年广东卷)(10分)C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用。请回答下列问题:
(1)Ge的原子核外电子排布式为
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3)按要求指出下列氧化物的空间构型、成键方式或性质
①CO2分子的空间构型及碳氧之间的成键方式 ;
②SiO2晶体的空间构型及硅氧之间的成键方式 ;
③已知SnO2是离子晶体,写出其主要物理性质 (写出2条即可)
CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为
(4)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060cm-1,CO分子中碳氧键的伸缩振动频率为2143cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度 (填字母)
A 强 B 弱 C 相等 D 无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com