
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | 生成l mol C的同时生成l mol D | D. | 气体的总物质的量 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、气体两边的计量数相等,反应过程中混合气体的压强始终不变,故A错误;
B、混合气体的密度不变,说明气体的质量不变,正逆反应速率相等,达平衡状态,故B正确;
C、都体现的正反应方向,未反映正与逆的关系,故C错误;
D、气体两边的计量数相等,反应过程中气体的总物质的量始终不变,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


科目:高中化学 来源: 题型:选择题
| A. | 将40 g NaOH固体溶解于1 L水中 | |
| B. | 将22.4 L氯化氢气体溶于水配成l L溶液 | |
| C. | 将l L 10 mol/L的浓盐酸与9 L水混合 | |
| D. | 20 g NaOH固体溶解在水中配成500 mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物.
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
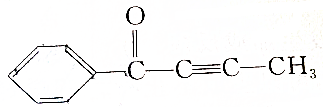 ,请回答下列问题:
,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 丙烷的球棍模型为 | |
| C. | 乙醇含有的官能团是-OH,带一个单位负电荷 | |
| D. | 乙酸的分子式为C2H4O2,其中CH3-在溶液中能电离出H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
)是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
 .
. .
. )是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号).
)是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号). +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 刚开始醋酸与锌反应速率大 | |
| B. | 反应过程中盐酸和醋酸分别与锌反应的速率一样大 | |
| C. | 醋酸与锌反应放出的氢气多 | |
| D. | 锌分别与醋酸、盐酸反应产生的氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加强汽车治理和垃圾处理场的建设和监管 | |
| B. | 实施“煤改气”、“煤改电”等清洁能源改造工程 | |
| C. | 研制新型高效可充电电池,发展纯电动汽车 | |
| D. | 加高工厂的烟囱,使烟尘和废气远离地表 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁:2MgO (熔融)$\stackrel{通直流电}{→}$Mg+O2↑ | B. | 钙:CaO+C$\stackrel{高温}{→}$Ca+CO↑ | ||
| C. | 锰:3MnO2+4Al$\stackrel{高温}{→}$3Mn+2Al2O3 | D. | 汞:HgS$\stackrel{加热}{→}$Hg+S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com