
���ĸ������ǩ���Լ�ƿ�У��ֱ�ʢ�����ᡢBaCl2��Һ��Na2CO3��Һ��AgNO3��Һ��Ϊ�˼����ƿ�е��Լ������Ƿֱ���ΪA��B��C��D��������ϣ���ʵ������Ϊ��A��B������ɫ���壻B��C������ɫ������A��D������ɫ������A��C�����Ա仯��
��1���ɴ��Ƴ����Լ�ƿ��ʢ���Լ�Ϊ���ѧʽ����
A��________��B��________��C________��D________��
��2��A��B��Ӧ�����ӷ���ʽΪ______________________________��
��3��A��D��Ӧ�����ӷ���ʽΪ______________________��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ����8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������X����(��ͨ��)Y��Һ�У����ɳ������������X�����ʵ�����ϵ��ͼ��ʾ ������ͼʾ�������( )
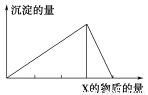
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ���ǣ� ��
A����̼�������Һ�м��������NaOH��Һ��Ca2++HCO3��+OH��=CaCO3��+H2O
B��KAl(SO4)2�еμ�Ba(OH)2ʹSO42��ǡ����ȫ������
2Al3++3 SO42��+3 Ba2++6 OH��=2Al(OH)3�� +3BaSO4��
C������������Һ��������SO2���壺SO2 + 2OH����SO32�� + H2O
D�����������ӹ���������Һ��Fe2+ + H2O2 + 2H+ Fe3+ + 4H2O
Fe3+ + 4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и�һ���£����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У�������ǣ� ��
A. Ԫ�����ڱ��У���18�����м���18����
B. ����������Ϊ2��Ԫ��ԭ�ӣ���һ�����ڢ�A��Ԫ��
C. �����ڱ��Ԫ�����ڵ�������������ԭ�Ӻ���ĵ��Ӳ���
D. ���������Ԫ�ض��ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и�һ���£����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�У�����ȱ��ֳ�ǿ�����ԣ��ֱ��ֳ����Ե��ǣ� ��
A��ϡ������п����Ӧ��������
B��Ũ����ʹ�������ۻ�
C��Ũ������ͭ��Ӧ���ȷ�Ӧ����SO2
D��Ũ�����ľ̿�ڼ��������·�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ��� ��
��Cl���Ľṹʾ��ͼ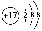
���ǻ��ĵ���ʽ��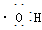 ��
��
��HClO�Ľṹʽ��H��Cl��O��
��NaHCO3��ˮ�еĵ��뷽��ʽ��NaHCO3=Na����H����CO32-��
��Na2O��ˮ��Һ�ܵ��磬�ⲻ��˵��Na2O�ǵ���ʣ�
��SiO2����������ᷴӦ������NaOH��Һ��Ӧ����SiO2�����������
�߷������ѻ����ǻ�ѧ�仯�� ��
A���٢ڢ� B���٢ܢޢ� C���ڢۢܢ� D���ڢۢݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ȡ100 mL 0��3 mol/L��300 mL 0��25 mol/L������ע��500 mL����ƿ�У���ˮϡ�����̶��ߣ��û����Һ��H�������ʵ���Ũ���ǣ� ��
A��0��21 mol/L B��0��42 mol/L C��0��56 mol/L D��0��26 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡЭ���������ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��25�桢101 kPa�����£�C��s����H2��g����CH3COOH��l����ȼ���ȷֱ�Ϊ393��5 kJ/mol��285��8 kJ/mol��870��3 kJ/mol����2C��s�� �� 2H2��g�� �� O2��g�� = CH3COOH��l���ķ�Ӧ��Ϊ�� ��
A����488��3 kJ/mol B����488��3 kJ/mol
C����191 kJ/mol D����191 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ����У������ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��t��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t��ʱAgCl��Ksp=4��10-10������˵������ȷ���ǣ� ��

A����t��ʱ��AgBr��KspΪ4��9��l0-13
B����AgBr������Һ�м���NaBr���壬��ʹ��Һ��c�㵽b��
C��ͼ��a���Ӧ����AgBr�IJ�������Һ
D����t��ʱ��AgCl��s��+Br-��aq�� AgBr��s��+Cl- ��aq����ƽ�ⳣ��K��816
AgBr��s��+Cl- ��aq����ƽ�ⳣ��K��816
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com