
【题目】有A、B、C、D四种元素,A元素的原子得两个电子,B元素的原子失去1个电子后所形成微粒均与氩原子有相同的电子层结构。C元素的原子只有1个电子,D元素原子的M电子层数比N层电子数多6个。试写出:
(1)A、B、C、D的元素符号和名称:A____ B____C____D____。
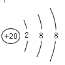
(2)A元素的原子结构示意图____,D元素的离子结构示意图:______。
(3)画出A离子的电子式____B原子的电子式____。
【答案】S硫 K钾 H氢 Ca钙 ![]()
![]()
![]()
【解析】
A元素的原子得两个电子,B元素的原子失去1个电子后所形成微粒均与氩原子有相同的电子层结构,A原子有16个电子,A是硫元素,B原子有19个电子,B是钾元素。C元素的原子只有1个电子,C是氢元素,D元素原子的M电子层数比N层电子数多6个,D原子N层有2个电子,M层有8个电子,D是钙元素。
(1)根据以上分析, A、B、C、D的元素符号和名称分别是:A是硫S 、B是钾K、C是氢H、D是钙Ca;
(2)A是S元素,核外有16个电子,原子结构示意图是![]() ,D元素的离子是Ca2+,核外有18个电子,结构示意图是
,D元素的离子是Ca2+,核外有18个电子,结构示意图是 ;
;
(3)A是S元素,S2-离子的电子式![]() ;B是K元素,钾原子最外层有1个电子,电子式是
;B是K元素,钾原子最外层有1个电子,电子式是![]() 。
。


科目:高中化学 来源: 题型:
【题目】能证明CH4的结构为空间正四面体而不是平面正方形的事实是)
A.CH3Cl的结构只有一种B.CH2Cl2的结构只有一种
C.CHCl3的结构只有一种D.CHCl4的结构只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法错误的是
A. “半江瑟瑟半江红”描述的是丁达尔效应
B. 由乙烯生产环氧乙烷的原子利用率可以为100%
C. 煤经气化、液化处理后再燃烧可有效减少酸雨形成
D. Na2O2作漂白剂时体现较强的氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠和钾的合金在常温下是液体,可用于快中子反应堆的热交换剂
B. 氯化铁、硫酸铁是优良的净水剂
C. 碳酸钡可作为检查肠胃的内服药剂,俗称“钡餐”
D. 乙醇可以直接作为燃料,也可以和汽油混合后作发动机燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项事实能说明上述观点的是
A. 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色
B. 丙烯和丙炔都能使溴水褪色
C. 等物质的量的乙醇和甘油与足量的金属钠反应,后者产生的氢气比前者多
D. 苯酚可以与NaOH反应,而环己醇不可以
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需精确配制480mL0.100mol/L的CuSO4溶液,以下操作正确的是
A.称取7.68gCuSO4,配成500mL溶液
B.称取12.0g胆矾,配成500mL溶液
C.称取8.0gCuSO4,加入500mL水
D.称取12.5g胆矾,配成500mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应N2(g)+3H2(g) ![]() 2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
2NH3(g )在10L的密闭容器中进行,测得2min内,N2的物质的量由20mol减小到8mol,则2min内NH3的反应速率为
A.1.2mol/(L·min)B.1.8mol/(L·min)
C.0.6mol/(L·min)D.0.4mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。已知:BCl3的熔点为-107.3℃,沸点为12.5℃,遇水水解生成H3BO3和HCl,请回答下列问题:
(实验Ⅰ)制备BCl3并验证产物CO

(1)该实验装置中合理的连接顺序为G→_____→_____→_____→____→F→D→I。其中装置E的作用是___________________________。
(2)装置J中反应的化学方程式为____________________________________。
(实验Ⅱ)产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。发生反应:Ag+ +SCN- =AgSCN↓。
⑤重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知: Ksp(AgCl)>Ksp(AgSCN) 。
(3)步骤④中达到滴定终点的现象为__________________。
(4)实验过程中加入硝基苯的目的是___________________。
(5)产品中氯元素的质量分数为_________________%。
(6)下列操作,可能引起测得产品中氯含量偏高是__________。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气与适量氯气混合反应可生成NH4Cl(俗称脑砂)和一种无污染的气体。某学习小组利用下列装置模拟该反应,请回答相关问题。

(1)该实验中所需的氯气是用浓盐酸与MnO2反应制取。装置A中仪器X的名称为____;X中发生反应的离子方程式为_______。
(2)要得到干燥纯净的氯气,上述A、B、C装置的连接顺序依次为a→_____(用小写字母表示)。
(3)利用E装置,将适量氨气与氯气充分混合反应氨气应从_______(用小写字母表示)通入,反应的化学方程式为_______________;可能观察到的现象是___________。
(4)《唐本草》记载脑砂入药可以散瘀消肿,天然脑砂含少量NH4Cl,现取天然脑砂进行NH4Cl含量测定。准确称取一定质量脑砂,与足量的氧化铜混合,如下图所示进行实验。已知:2NH4Cl+3CuO=3Cu+N2+2HCl+3H2O 。
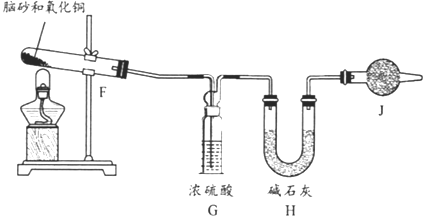
①为顺利完成有关物理量的测定,请完善下列表格:
测量时间点 | 加热前 | 当观察到_____现象时 |
测量内容 | _______________ | 停止加热,冷却,称量H装置的总质量 |
②如果不用J装置,测出NH4Cl的含量将_____(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com