
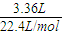 =0.3mol,若Br-不参加反应,则原溶液中n(Fe2+)=
=0.3mol,若Br-不参加反应,则原溶液中n(Fe2+)= n(Br-)=
n(Br-)= ×0.3mol=0.15mol,0.15molFe2+被氧化提供的电子为0.15mol,3.36LCl2反应获得的电子的物质的量2×
×0.3mol=0.15mol,0.15molFe2+被氧化提供的电子为0.15mol,3.36LCl2反应获得的电子的物质的量2×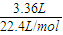 =0.3mol,大于0.15molFe2+被氧化转移的电子为0.15mol,故Br-参加反应,氯气完全溶液后溶液为中溶质为FeBr3、FeCl3,根据铁元素守恒可知n(Fe3+)=
=0.3mol,大于0.15molFe2+被氧化转移的电子为0.15mol,故Br-参加反应,氯气完全溶液后溶液为中溶质为FeBr3、FeCl3,根据铁元素守恒可知n(Fe3+)= n(Cl-)+
n(Cl-)+ n(Br-),故原溶液中n(FeBr2)=n(Fe3+),再根据c=
n(Br-),故原溶液中n(FeBr2)=n(Fe3+),再根据c=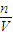 计算.
计算.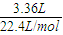 =0.3mol,
=0.3mol, n(Br-)=
n(Br-)= ×0.3mol=0.15mol,0.15molFe2+被氧化提供的电子为0.15mol,3.36LCl2反应获得的电子的物质的量2×
×0.3mol=0.15mol,0.15molFe2+被氧化提供的电子为0.15mol,3.36LCl2反应获得的电子的物质的量2×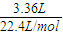 =0.3mol,大于0.15molFe2+被氧化转移的电子为0.15mol,
=0.3mol,大于0.15molFe2+被氧化转移的电子为0.15mol, n(Cl-)+
n(Cl-)+ n(Br-)=
n(Br-)= ×0.3mol+
×0.3mol+ ×0.3mol=0.2mol,
×0.3mol=0.2mol,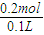 =2mol/L.
=2mol/L.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)已知①氯水和溴水能将Fe2+氧化成Fe3+,而碘水不能;②Fe3+可以使KI—淀粉试液变蓝色。
(1)向100mlFeBr2溶液中通入标况下体积为3.36L的Cl2,充分反应后测得溶液中Cl—和Br—的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为 ;
(2)向含1molFeI2和2molFeBr2的溶液中通入3molCl2后,溶液中所含各种离子的个数之比是 ;
(3)向含a mol FeI2和b mol FeBr2的溶液中通入c molCl2,若要保证溶液中含有两种阳离子,
c的取值范围是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省石家庄市高三暑期第二次考试化学试卷(解析版) 题型:选择题
已知2Fe2++Br2=2Fe3++2Br-。向100mlFeBr2溶液中通入标准状况下的Cl2 3.36L,充分反应后测得溶液中Cl-与Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为
A. 2mol/L B. 1mol/L C. 0.4mol/L D. 0.2mol/L
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省高三第二次模拟考试化学试卷 题型:选择题
向100mLFeBr2溶液中通入标准状况下的C12 3.36 L,C12全部被还原,测得溶液中c(Br–)=c(C1–),则原FeBr2溶液的物质的量浓度是( )
A. 2mol/L B. 3 mol/ L C.1.5 mol/ L D. 0.75mol/L
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
 SO2Cl2(l) △H = -97.3 kJ . mol-1
SO2Cl2(l) △H = -97.3 kJ . mol-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com