
 $→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$→_{过滤}^{调节PH_{3}-4}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O $\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O
$\stackrel{40℃-50℃}{→}$CuSO4溶液$→_{过滤}^{结晶}$CuSO4•5H2O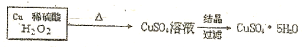 .
.
分析 (1)灼烧固体应在坩埚中进行,据此答题;
(2)亚铁离子能被空气中的氧气氧化成铁离子,调节pH值要能与酸反应且不引入新的杂质,同时不能使铜离子沉淀;
(3)①Cu与稀硫酸和稀硝酸混合,为了只得到CuSO4溶液,硝酸只能全部做氧化剂生成一氧化氮,根据电子得失守恒可计算硝酸的物质的量;
②根据反应的条件可判断加热方式,硝酸易挥发,所以要冷凝回流,同时导管能导气;
③NO难溶于水,可以用排水法收集,反应的尾气为NO,要与氧气反应后才能被氢氧化钠吸收,据此选择装置;
(4)根据题中提供的药品可知,实验室制备CuSO4•5H2O较好的方法是在硫酸溶液中用双氧水氧化铜,为保证反应速率可适当加热,得硫酸铜溶液后再通过蒸发浓缩、降温结晶、过滤得CuSO4•5H2O,据此答题.
解答 解:(1)灼烧固体应在坩埚中进行,
故答案为:坩埚;
(2)亚铁离子能被空气中的氧气氧化成铁离子,反应的离子方程式为4H++O2+4Fe2+═4Fe3++2H2O,调节pH值要能与酸反应且不引入新的杂质,同时不能使铜离子沉淀,所以加入的试剂为CuO、CuCO3、Cu(OH)2等,
故答案为:4H++O2+4Fe2+═4Fe3++2H2O;CuO、CuCO3、Cu(OH)2;
(3)①Cu与稀硫酸和稀硝酸混合,为了只得到CuSO4溶液,硝酸只能全部做氧化剂生成一氧化氮,根据电子得失守恒可知,1mol硝酸能氧化1.5mol铜,同时也消耗1.5mol硫酸,所以100mLl.0moI•L-1稀硝酸即含有0.1mol硝酸中加入1.0mol•L-1稀硫酸的体积为150mL,
故答案为:150;
②该反应的条件为40℃-50℃,所以可以用水浴加热的方式,硝酸易挥发,所以要用圆底烧瓶上方长导管冷凝回流,同时导管能导气,
故答案为:水浴加热;导气兼冷凝回流;
③NO难溶于水,可以用排水法收集,反应的尾气为NO,要与氧气反应后才能被氢氧化钠吸收,所以选择AC装置,
故答案为:AC;
(4)根据题中提供的药品可知,实验室制备CuSO4•5H2O较好的方法是在硫酸溶液中用双氧水氧化铜,为保证反应速率可适当加热,得硫酸铜溶液后再通过蒸发浓缩、降温结晶、过滤得CuSO4•5H2O,所以实验方案的流程图为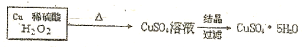 ,
,
故答案为: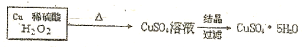 .
.
点评 本题以以Cu为原料制取CuSO4•5H2O为载体考查了实验基本操作、实验原理分析、实验方案的设计等,题目综合性强,难度中等,答题时注意元素化合物质的基础知识的灵活运用.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图①是pH=13的NaOH溶液中加水稀释 | |
| B. | 图②是用适量的KClO3和MnO2混合物加热制O2 | |
| C. | 图③是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 图④向一定质量的稀盐酸中加入铁粉至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W | R |
| 相 关 信 息 | 能形成+7价的化合物 | 日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子,它是空气的主要成分之一 | 焰色反应为黄色 | 位于第ⅣA族,是形成化合物种类最多的元素 |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置中铜是负极 | |
| B. | 铜表面的反应为:2H++2e-=H2↑ | |
| C. | 电流的方向是从铁经导线流向铜 | |
| D. | 构成原电池后,铁与硫酸铜的反应速率加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com