
A.4.6 g Na投入45.4 g水中
B.6.2 g Na2O投入43.8 g水中
C.7.8 g Na2O2投入42.2 g水中
D.8 g NaOH投入42 g水中
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
 某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)某活动课程小组拟用50 mLNaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
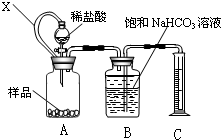
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放的试剂是_____ _,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省开封市高一上学期期中考试化学试卷 题型:填空题
(10分)为测定氯化钾和硫酸钾混合物中氯化钾的含量,某同学设计了如下实验:称量样品,溶解,添加适量A溶液,过滤,得沉淀和滤液B,将沉淀洗涤,烘干,得物质C。
回答下列问题:
(1)溶液A溶质的化学式_____,物质C的化学式____。
(2)用托盘天平称量样品,当天平平衡时,发现左盘错放砝码质量为26g,游码为0.4g,则右盘样品实际质量是____。
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是______。
(4)若C的质量为 23.3g,则原混合物中氯化钾的质量分数为______。
23.3g,则原混合物中氯化钾的质量分数为______。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省济宁市邹城二中高一上学期期中质量检测化学试卷 题型:实验题
(10分)某活动课程小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤:
a.取25 mL  NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;
b.小火煮沸溶液1~2 min,赶走溶解在溶液中的CO2气体;
c.在得到的溶液中加入另一半(25 mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出c步骤的离子方程式_________________.
此方案第一步的实验装置如下图所示:
(2)加入反应物前,如何检验整个装置的气密性:________________________ ________________________________________________
(3)若用大理石与盐酸制CO2,则装置B中盛放 的试剂是_____
的试剂是_____  _,作用是_____________________________________________
_,作用是_____________________________________________
(4)在实验室通常制法中,装置A还可作为下列______ (填序号)气体的发生装置.
①HCl ②H2 ③O2 ④NH3
(5)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶液密度为1.44 g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为_______ mol/L.
查看答案和解析>>
科目:高中化学 来源:2014届上海市七校高二5月阶段检测化学试卷(解析版) 题型:计算题
A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含一种官能团,且每个碳原子上最多只连一个官能团;A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。通过计算求:
(1)A的分子式是_____________(写出计算过程),其结构简式是____________________。
(2)写出A与乙酸反应的化学方程式:________________________________________。
(3)27.2gA在空气中充分燃烧时至少需要空气(标况下)多少L;生成的CO2用170ml 10mol/L的NaOH溶液吸收,反应后溶液中溶质的成分是什么,其物质的量各是多少?
(4)写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。写出这些同分异构体的结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com