
| n |
| V |
| 0.92g |
| 23g/mol |
| n |
| V |
| 0.04mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、pH=12的溶液:Ca2+、NH4+、Br-、HSO3- |
| B、无色溶液:K+、Al3+、HCO3-、Cl- |
| C、通入H2S无沉淀:Cu2+、Na+、I-、SO42- |
| D、c(H+)=1×10-2mol/L的溶液:Fe3+、Ba2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | H2CO3 | H2SO3 | HClO |
| 电离平衡常数 (25℃) |
K1=4.30×l0-7 | K1=1.54×l0-2 | K=2.95×l0-8 |
| K2=5.61×l0-11 | K2=1.02×l0-7 |
| A、ClO-+CO2+H2O→HClO+HCO3- |
| B、SO32-+CO2+H2O→HSO3-+HCO3- |
| C、2ClO-+SO2+H2O→2HClO+SO32- |
| D、2HSO3-+CO32-→2SO32-+CO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 有多种同分异构体,其中苯环上只有一个侧链的同分异构体的结构简式是
有多种同分异构体,其中苯环上只有一个侧链的同分异构体的结构简式是查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| R | ||
| T | X |
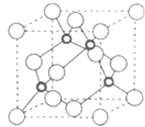
查看答案和解析>>
科目:高中化学 来源: 题型:
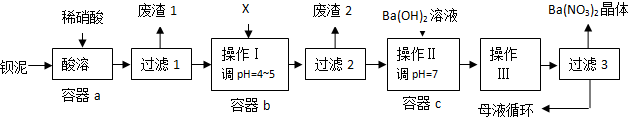
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com