


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源:不详 题型:单选题
| A.X最高价氧化物对应的水化物不一定是强酸 |
| B.X元素的氢化物化学式一定为H2X |
| C.X的单质—定是良好的半导体材料 |
| D.X元素的氧化物—定能与烧碱反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳酸钡的溶解度略大于硫酸钡,向硫酸钡的饱和溶液中加入较多的碳酸钠固体,会有碳酸钡生成 |
B.某温度T时,水的离子积常数为KW,该温度下将V1mLa mol?L-1的一元酸HA与V2mLb mol?L-1的一元碱BOH充分混合,若混合溶液中c(OH-)= mol?L-1,则此溶液不一定呈中性 mol?L-1,则此溶液不一定呈中性 |
| C.ⅣA族元素形成的氢化物的沸点从上到下依次递增,则ⅤA族元素所形成的氢化物的沸点从上到下也是依次递增 |
D.依据反应2C+SiO2 2CO↑+Si ,还原性:Si <C 2CO↑+Si ,还原性:Si <C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

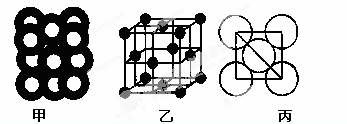
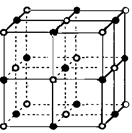
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②③④ | C.①②⑤ | D.①②④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | W | |
| X | Y | Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.86 | B.222 | C.136 | D.50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com