
下列有关实验装置进行的相应实验,能达到实验目的的是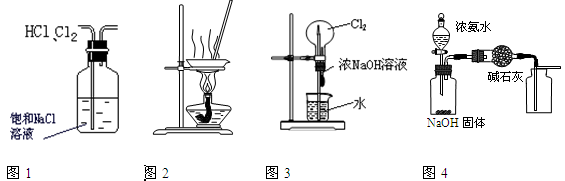
| A.用图1所示装置除去HCl中含有的少量Cl2 |
| B.用图2所示装置蒸发FeCl3溶液制备无水FeCl3 |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置制取并收集干燥纯净的NH3 |
科目:高中化学 来源: 题型:单选题
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是(考查每一个操作时,假设其它操作均正确)( )
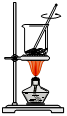 | 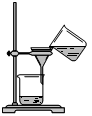 |  | 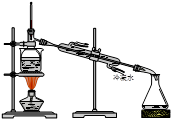 |
| A.海带灼烧成灰 B.过滤得含I-溶液 C.放出碘的苯溶液 D.分离碘并回收苯 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验装置进行的相应实验,能达到实验目的的是
| A.装置甲可用于检验有乙烯生成 |
| B.装置乙可用于收集和吸收氨气 |
| C.装置丙可用于除去CO2中混有的HCl气体 |
| D.装置丁可用于除去溴苯中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
见下表。欲用一种试剂甲来检验其溶液中的离子X,在同时有离子Y存在时,此检验仍可进行的是(在实验过程中不允许加热.过滤.萃取……等操作)
| | 试剂甲 | 离子X | 离子Y |
| A | HCl.Ba(OH)2 | CO32- | HCO3- |
| B | NH3 .H2O | Al3+ | Mg2+ |
| C | AgNO3 | I- | Cl- |
| D | NH4SCN,氯水 | Fe2+ | Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
实验室制浓硫酸、浓硝酸的混合物与苯反应制取硝基苯。得到粗产品后,要选用如下几步操作对粗产品进行精制:①蒸馏 ②水洗 ③用干燥剂进行干燥 ④用10%的NaOH溶液洗涤。正确的操作步骤是
| A.①②③④② | B.②④②③① | C.④②③①② | D.③④①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验的结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 溶液中一定含有 |
| B | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体 | 溶液中一定含有 |
| C | 用酸度计测定SO2和CO2饱和溶液的pH,前者pH小 | H2SO3酸性强于H2CO3 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
TiO2在工业生产和日常生活中有重要用途。
(1)工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的主要反应为:2H2SO4+FeTiO3 ="=" TOSO4(硫酸氧钛)+FeSO4+2H2O
净化钛矿石时,需用浓氢氧化钠溶液来处理。写出该过程中发生反应的化学方程式:________________。
步骤③中加热的目的是(请写出必要的化学方程式和文字): 。
(2)用TiO2制备金属钛的一种方法是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti。因下述反应难于发生:TiO2(s)+2Cl2(g) TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。
TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。
已知:C(s)+O2(g)=CO2(g) △H= 394 kJ/mol。
394 kJ/mol。
则TiO2(s)+C(s)+2Cl2(g)=TiCl4(1)+CO2(g) △H=________
从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因是_______________。
(3)下图是一种染料敏化太阳能电池的示意图。电池的一个由有机光敏染料(S)涂覆TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
TiO2/S TiO2/S*(激发态)
TiO2/S*(激发态)
TiO2/S*  TiO2/S+ + e-
TiO2/S+ + e-
I3-+2e- 3I-
3I-
2TiO2/S*+I3-  2TiO2/S + I3-
2TiO2/S + I3-
下列关于该电池叙述正确的是
| A.电池工作时,I-离子在镀铂导电玻璃电极上放电 |
| B.电池工作时,是将太阳能转化为电能 |
| C.电池的电解质溶液中I-和I3- 浓度不会减少 |
| D.电池中镀铂导电玻璃为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)Ⅰ 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答下列问题。(1)乙烯的电子式____________,结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸 B.溴的四氯化碳溶液 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2
Ⅱ 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。
(1)乙醇分子官能团名称是__________________。
(2)试管a中加入几块碎瓷片的目的是____________。
(3)试管a中发生反应的化学方程式为___________,反应类型是________________________。
(4)反应开始前,试管b中盛放的溶液是____________。作用是 。
(5)可用____________的方法把制得的乙酸乙酯分离出来。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com