
【题目】某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中说法不正确的是( )
A.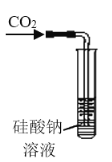 可用来证明碳的非金属性比硅强
可用来证明碳的非金属性比硅强
B.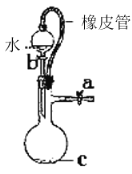 橡皮管的作用是能使水顺利流下
橡皮管的作用是能使水顺利流下
C. 用图示的方法不能检查此装置的气密性
用图示的方法不能检查此装置的气密性
D. 先从①口进气集满CO2,再从②口进气,可收集NO
先从①口进气集满CO2,再从②口进气,可收集NO
【答案】C
【解析】
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
B.利用压强差将液体顺利流下;
C.能产生压强差的装置能检验装置气密性;
D.常温下二氧化碳和NO不反应,可以采用排二氧化碳法收集NO。
A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,二氧化碳和硅酸钠溶液反应生成硅酸,说明碳酸酸性大于硅酸,碳酸、硅酸都是其最高价氧化物的水化物,所以非金属性C>Si,故A正确;
B.产生的气体通过橡皮管进入分液漏斗上部,导致分液漏斗上部和烧瓶内气体产生压强差,所以利用压强差将液体顺利流下,故B正确;
C.该装置能通过调节乙能产生压强差,所以能利用该装置检验装置气密性,故C错误;
D.常温下二氧化碳和NO不反应,可以采用排二氧化碳法收集NO,二氧化碳密度大于NO,所以该采用向下排二氧化碳法收集NO,则先从①口进气集满二氧化碳,再从②口进气,可收集NO,故D正确;
故答案选C。


科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应A(气)+3B(气)![]() 2C(气)若达到平衡的标志是
2C(气)若达到平衡的标志是
A. C的生成速率与B的生成速率相等
B. A、B、C的浓度不再发生变化
C. 单位时间内生成nmolA,同时生成3nmolB
D. A、B、C的分子数之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法中合理的是( )

A. 可以选用方案1分离碳酸氢钠中含有的氯化铵
B. 方案1中的残留物应该具有的性质是受热易挥发
C. 方案2中加入的试剂一定能够与除X外的物质发生化学反应
D. 方案2中加入NaOH溶液可以分离出SiO2和Fe2O3混合物中的Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的发明是化学对人类的一项重大贡献。
I:如图所示,烧杯中都盛有稀硫酸。
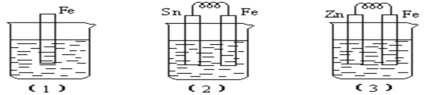
(1)中反应的离子方程式为______________,
(2)中的电极反应:Fe:______________、Sn:______________Sn极附近溶液的pH______________(填增大、减小或不变),
(3)中被腐蚀的金属是______________、比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是______________
II:依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+ 设计的原电池如图所示。
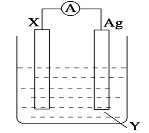
(1)电极 X 的材料是_____;电解质溶液 Y 是_____。
(2)Ag 电极上发生的反应为:_________。
(3)针对上述原电池装置,下列说法中不正确的是_____。(双选)
A.原电池工作时的总反应:Cu+2Fe3+=2Fe2++Cu2+
B.原电池工作时,X 电极流出电子,发生氧化反应
C.原电池工作时,银电极上发生氧化反应
D.原电池工作时,阴离子向 Ag 极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组有机化合物中,不论两者以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变的是
A. CH4O,C3H4O5B. C3H6,C3H8O
C. C3H8,C4H6D. C2H6,C4H6O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是( )
A. 用氯苯合成环己烯:![]()
B. 用甲苯合成苯甲醇:![]()
C. 用乙烯合成乙酸:![]()
D. 用乙烯合成乙二醇:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构或性质的描述,不正确的是
A. C4H9OH发生催化氧化反应,可生成3种有机产物
B. 光照下,Cl2可在甲苯的苯环上发生取代反应
C. 异戊二烯可发生加聚反应,生成高分子化合物
D. 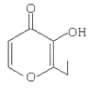 的分子式为C7H8O3
的分子式为C7H8O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:
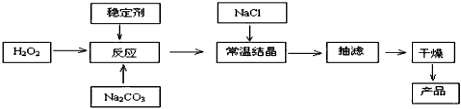
已知:2Na2CO3 + 3H2O2 =2Na2CO3·3H2O2 △H<0
请回答下列问题:
(1)下列物质可使过碳酸钠较快失效的是_________________。
a.MnO2 b.H2S c.稀硫酸 d.NaHCO3
(2)加入NaCl的作用是_________________。
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是_________________。
(4)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是_________________。
(5)以上流程中遗漏了一步,造成所得产品纯度偏低,该步操作的名称是_________________。进行该操作的方法是:_________________。
(6)为测定产品的纯度。
准确称取ag产品配成250mL溶液,移取25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释成100mL,作被测试样;用高锰酸钾标准溶液滴定被测试样,MnO4-的还原产物是Mn2+。用cmol/L KMnO4标准溶液VmL滴定待测液,滴定到达终点的现象是________________。
重复滴定三次,平均消耗cmol/L KMnO4标准溶液VmL,则产品中过碳酸钠的质量分数为______________。配制cmol/L KMnO4标准溶液时,移液时有少量液体溅出,则产品的纯度将_________(变大、变小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉煤灰中的氮可通过如图所示方法处理生成对环境无影响的氮气,下列说法正确的是
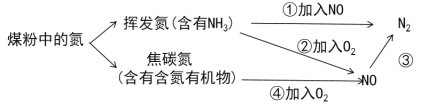
A.反应③中加入的物质可以是空气或氨气
B.反应①中,每生成22.4L(标况下)N2,转移电子2.4mol
C.用湿润的蓝色石蕊试纸可判断挥发氮中含有NH3
D.焦碳氮在空气中充分燃烧产生的尾气可直接排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com