
| A、0.18 | B、0.3 |
| C、0.6 | D、0.45 |
科目:高中化学 来源: 题型:
| A、得电子数越多的物质氧化性越强 |
| B、化合反应或分解反应有可能是氧化还原反应 |
| C、离子反应也可以是氧化还原反应 |
| D、氧化还原反应的实质是发生电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO的摩尔质量为28 |
| B、常温常压下,NA个氢原子与NA 个氮气的质量比为1:14 |
| C、32克O2所含原子数目为2NA |
| D、常温常压下,1molCO分子所占体积是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(OH)2=Ba2++(OH)22- |
| B、H2SO4=H++HSO4- |
| C、NaHCO3=Na++HCO3- |
| D、Al2(SO4)3=Al3++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:1 |
| C、2:3 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7种 | B、8种 | C、6种 | D、12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
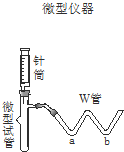 现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动:
现有一瓶实验室放置已久的可能被氧化的Na2SO3固体,为了研究它的组成,请你参与同学们进行的如下探究活动:| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量固体样品于微型试管中;在W管a处滴入 | |
| 步骤2:用针筒吸入 | |
| 步骤3:拨出针筒,吸入蒸馏水洗净;再吸入 | . |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com