
以钡矿粉(主要成份为BaCO3,含有Ca2+、Fe2+、Fe3+、Mg2+等)制备BaCl2·2H2O的流程如下:

(1)氧化过程主要反应的离子方程式为 。
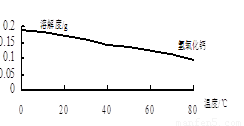
(2)沉淀C的主要成分是Ca(OH)2和 。由图可知,为了更好的使Ca2+沉淀,还应采取的措施为 。


(3)用BaSO4重量法测定产品纯度的步骤为:
步骤1:准确称取0.4~0.6 g BaCl2·2H2O试样,加入100 ml 水,3 ml 2 mol·L-1 的HCl溶液加热溶解。
步骤2:边搅拌,边逐滴加入0.1 mol·L-1 H2SO4溶液。
步骤3:待BaSO4沉降后, ,确认已完全沉淀。
步骤4:过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。
步骤5:将折叠的沉淀滤纸包置于 中,经烘干、炭化、灰化后在800℃灼烧至恒重。称量计算BaCl2·2H2O中Ba2+的含量。
①步骤3所缺的操作为 。
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为 。
③步骤5所用瓷质仪器名称为 。滤纸灰化时空气要充足,否则BaSO4易被残留的炭还原生成BaS,该反应的化学方程式为 。
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因 。
[已知:Ksp(BaSO4)=1.1×10-10 Ksp(BaCrO4)=1.2×10-10]
(1)H2O2+ 2Fe2++2H+ =2Fe3+ +2H2O
(2)Mg(OH)2 提高温度
(3)①向上层清液中加入1~2滴0.1mol/LH2SO4溶液
②称取试样过少,沉淀量就少,洗涤造成的损失就大
③坩埚
BaSO4 + 4C 4CO +
BaS或BaSO4 + 2C
4CO +
BaS或BaSO4 + 2C 2CO2 + BaS
2CO2 + BaS
④BaCrO4的摩尔质量大于BaSO4
【解析】
试题分析:该题为化工流程题,以主要成分为BaCO3钡矿粉,经过除去含有Ca2+、Fe2+、Fe3+、Mg2+等杂质制备BaCl2·2H2O的流程。(2)沉淀C之前已除去铁,所以该步是除去剩余的杂质Ca2+、Mg2+,生成相应氢氧化物;由图看到,Ca(OH)2溶解度随温度升高而降低,故高温下有利于Ca2+除净;(3)①步骤3显然是确定沉淀是否完全的操作,应该是静置,向向上层清液中加入1~2滴原H2SO4溶液,若不出现沉淀,则Ba2+沉淀完全;②称取试样过少,沉淀量就少,洗涤造成的损失就大;③固体灼烧一般都在坩埚中;④两种物质的Ksp几乎相同,但BaCrO4的摩尔质量大于BaSO4,实验中生成的沉淀的质量大,误差小。
考点:化工流程题,考查物质的分离、除杂、检验、实验分析等基本实验操作的有关问题。


 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省高考重点命题预测系列化学试卷(解析版) 题型:实验题
以钡矿粉(主要成份为BaCO3,含有Ca2+、Fe2+、Fe3+、Mg2+等)制备BaCl2·2H2O的流程如下:

(1)氧化过程主要反应的离子方程式为 。
(2)沉淀C的主要成分是Ca(OH)2和 。
由图可知,为了更好的使Ca2+沉淀,还应采取的措施为 。

(3)用BaSO4重量法测定产品纯度的步骤为:
步骤1:准确称取0.4~0.6 g BaCl2·2H2O试样,加入100 ml 水,3 ml 2 mol·L-1 的HCl溶液加热溶解。
步骤2:边搅拌,边逐滴加入0.1 mol·L-1 H2SO4溶液。
步骤3:待BaSO4沉降后, ,确认已完全沉淀。
步骤4:过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。
步骤5:将折叠的沉淀滤纸包置于 中,经烘干、炭化、灰化后在800℃灼烧至恒重。称量计算BaCl2·2H2O中Ba2+的含量。
①步骤3所缺的操作为 。
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为 。
③步骤5所用瓷质仪器名称为 。滤纸灰化时空气要充足,否则BaSO4易被残留的炭还原生成BaS,该反应的化学方程式为 。
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因 。
[已知:Ksp(BaSO4)=1.1×10-10 Ksp(BaCrO4)=1.2×10-10]
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com