
【题目】生产中常要控制化学反应条件增大反应速率。下列措施中不能加快化学反应速率的是
A. 尽可能使用稀溶液 B. 选择合适的催化剂
C. 碾细固体反应物 D. 提高反应体系的温度
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+、Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
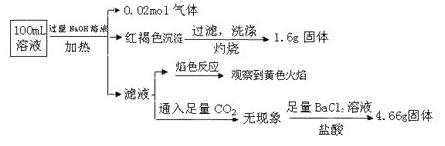
下列说法正确的是( )
A. 原溶液中c(Fe3+)=0.2 molL-1
B. 溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
C. SO42ˉ、NH4+、Na+一定存在,CO32ˉ一定不存在
D. 要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,有甲、乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲、乙两容器中加入6molA和3molB,发生反应如下:3A(g)+bB(g)![]() 3C(g)+2D(g)ΔH<0;4min时甲容器内的反应恰好达到平衡,
3C(g)+2D(g)ΔH<0;4min时甲容器内的反应恰好达到平衡,
A的浓度为2.4mol/L,B的浓度为1.8mol/L;tmin时乙容器内的反应达平衡,
B的浓度为0.8mol/L.根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)=______________。
(2)乙容器中反应达到平衡时所需时间t__________4 min(填“大于”、“小于”或“等于”)。
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是______________。
A.保持温度不变,增大甲容器的体积至2 L
B.保持容器体积不变,使甲容器升高温度
C.保持容器体积和温度都不变,向甲中加入一定量的A气体
D.保持容器体积和温度都不变,向甲中加入一定量的B气体
(4)该温度下,向体积为1L的密闭容器中通入A、B、C、D气体物质的量分别为3mol、1mol、3mol、2mol,此时反应________________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”))
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是
A.增大反应物的浓度,活化分子百分数增加,反应速率加快
B.增大气体反应体系的压强,单位体积中活化分子数增多,气体反应速率加快
C.升高反应的温度,活化分子百分数增加,有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有非常丰富的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源综合利用的示意图。
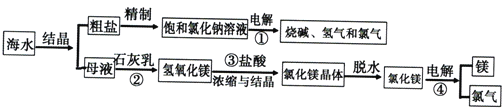
试回答下列问题:
(1)反应①、②、③、④中,属于氧化还原反应的是__________。
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,有人设计如下方案:先将粗盐溶于水,再加入过量的氢氧化钠溶液,然后进行下列四项操作:a.过滤;b.加适量的盐酸;c.加过量的碳酸钠溶液;d.加过量的氯化钡溶液,该四项合理的操作顺序为______(每个操作仅用一次,用a、b、c、d符号填写)
(3)请写出反应①的化学方程式_______________。
(4)请写出反应③的离子方程式_______________。
(5)母液中通入氯气,还可以制备溴单质,该反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
①2Cu(s)+![]() O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
②C(s)+![]() O2===CO(g) ΔH=-110.5 kJ·mol-1,
O2===CO(g) ΔH=-110.5 kJ·mol-1,
③2Cu(s)+ O2(g)===2CuO(s) ΔH=-314 kJ·mol-1
(1)则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为______________________。
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。

请回答下列问题:
①甲池为__________(填“原电池”“电解池”或 “电镀池”),A电极的电极反应式为______________
②丙池中电池总反应的离子方程式:_______________________
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为______mL(标准状况)。
④一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.CuO B. Cu C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是 ( )
3C+4D反应中,表示该反应速率最快的是 ( )
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯,交通及日常生活中有着广泛的应用。
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是( )
2Ni(OH)2+Cd(OH)2。已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是( )
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
A.①③ B.②④
C.①④ D.②③
(2)废弃的镍镉电池已成为重要的环境污染物,有资料表明一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重。这是因为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅, 当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为
A. 0.05mol B. 1mol C. 1.05mol D. 0.13mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com