
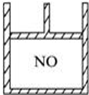
 如图所示,在装有活塞的密闭容器内盛22.4mL NO,若通入11.2mL O2(气体体积均在标准状况下测定),保持温度、压强不变,则容器内混合气体的密度( )
如图所示,在装有活塞的密闭容器内盛22.4mL NO,若通入11.2mL O2(气体体积均在标准状况下测定),保持温度、压强不变,则容器内混合气体的密度( )| 0.0224L |
| 22.4L/mol |
| 0.0112L |
| 22.4L/mol |
| 0.0224L |
| 22.4L/mol |
| 0.0112L |
| 22.4L/mol |
| 0.046g |
| 0.0224L |
| 0.046g |
| 0.0112L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
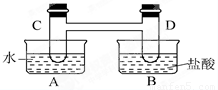
 I、如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2?N2O4△H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:
I、如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2?N2O4△H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:查看答案和解析>>
科目:高中化学 来源: 题型:013
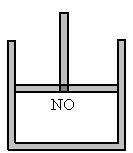
如图所示是一个装有活塞的密闭容器,内盛22.4mL一氧化氮气体,若向密闭容器中通入11.2mL氧气(气体体积均在标准状况下测定).保持温度、压强不变,则容器内的密度是
[ ]
A.等于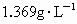 B.等于
B.等于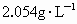
C.在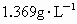 和
和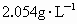 之间
D.大于
之间
D.大于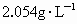
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
如图所示是一个装有活塞的密闭容器,内盛22.4mL一氧化氮气体,若向密闭容器中通入11.2mL氧气(气体体积均在标准状况下测定).保持温度、压强不变,则容器内的密度是
[ ]

A.等于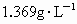 B.等于
B.等于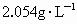
C.在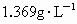 和
和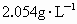 之间
D.大于
之间
D.大于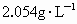
查看答案和解析>>
科目:高中化学 来源:2012-2013学年吉林省长春外国语学校高二(上)期中化学试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com