
在80℃时,某物质在2L的容器中发生化学反应,隔一段时间对该容器内的物质进行分析,得到如表数据:
则下列说法正确的是
A.该反应的方程式为2NO2 N2O4
B.80s前该反应一定没有达到平衡状态
C.a的取值为0.56
D.20s到40s内用N2O4表示的反应速率为0.010mol·L-1·S-1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 浓H2SO4△ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、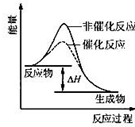 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | B、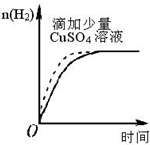 表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线) 表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线) | C、 表示 KNO3的溶解度曲线,a点所示的溶液是 80℃时 KNO3 的不饱和溶液 表示 KNO3的溶解度曲线,a点所示的溶液是 80℃时 KNO3 的不饱和溶液 | D、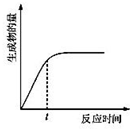 表示某可逆反应生成物的量随反应时间变化的曲线,t 时反应物转化率最大 表示某可逆反应生成物的量随反应时间变化的曲线,t 时反应物转化率最大 |
查看答案和解析>>
科目:高中化学 来源:2014届山东省聊城市七校联考高二上学期期末检测化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是

A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.图2表示0.1000 mol·L-1NaOH溶液滴定20.00 mL 0.1000 mol·L-1CH3COOH溶液所得到的滴定曲线
C.图3表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液
D.图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时刻反应物转化率最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com