
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
|
离子 |
K+ |
Na+ |
NH4+ |
SO42- |
NO3- |
Cl- |
|
浓度/mol.L |
4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据判断PM2.5的酸碱性为 ,试样的pH值 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)=H2O(g)
 H= -241.8KJ/mol
H= -241.8KJ/mol
C(s)+1/2O2(g)=CO(g)  H= -110.5KJ/mol
H= -110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式 ;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 ;
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g)
2NO(g)  H>0
H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡。测得NO为8×10-4mol.计算该温度下的平衡常数K= ___________;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g)已知该反应的 H>0,简述该设想能否实现的依据 。
H>0,简述该设想能否实现的依据 。
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 。
(1)酸性;4;
(2)①C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3KJ/mol;②a、b;
(3)①4×10-6;温度越高,反应速率加快,平衡右移;②该反应是焓增,熵减的反应,任何温度下均不自发进行;③2CO+2NO 2CO2+N2
2CO2+N2
【解析】
(1)考查溶液中的电荷守恒具体计算,c(K+)+ c(H+)+ c(Na+)+c(NH4+)= c(OH—)+ 2 c(SO42—)+2 c(NO3—)+ cCl—),而c(OH—)·c(H+)=10-14,代入具体数据计算可得:c(OH—)=10-10mol/L,c(H+)=10-4 mol/L;
(2)①由盖斯定律,两式相加可得:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3KJ/mol;②吸收SO2可用ab;
(3)①由题目未告诉容器体积,不妨令为1L注意近似处理,平衡时: c(N2)=0.8mol/L,
c(O2) ="0.2mol/L," ,c(NO)=8×10-8mol/L,将数据代入K=c2(NO)÷[c(N2)·c(O2)]=
4×10-6;因为该反应为吸热反应,温度越高,反应速率加快,平衡右移;②该反应是焓增,熵减的反应,由ΔG=ΔH-TΔS,任何温度下均不自发进行;③产物为N2和CO2才无污染:2CO+2NO 2CO2+N2
2CO2+N2
【规律提升】(1)溶液中的守恒规律要能够灵活运用,pH计算式不要忽略水的离子积,并看清温度限制;(2)盖斯定律的运功要学会加减法的运用,符号不要弄反;(3)平衡常数有关计算时,近似处理(两个数相加减相差100倍以上,可以忽略小的数)、假设处理(例如假设体积)、三阶段式等比较重要;(4)利用ΔG=ΔH-TΔS判断反应进行方向一定不要把符号弄反。
【考点定位】本题以PM2.5等环保知识为背景,综合考查反应原理部分内容,具体如下:(1)电荷守恒、pH计算、盖斯定律计算、SO2吸收问题、平衡常数计算、反应进行方向的判断、信息方程式的书写等。


科目:高中化学 来源: 题型:阅读理解
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 离子 | H+ | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol?L-1 | 未测定 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省滦南一中高二下学期期末考试化学试卷(带解析) 题型:填空题
根据所学知识,完成下列问题:
(1)化学反应可视为旧键断裂和新键生成的过程。键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和其燃烧产物P4O6的分子结构如图所示,现提供以下键能(kJ· mol-1): P-P:198, P-O:360, O-O:498,白磷(P4)燃烧的热化学方程式为 。
(2)化学能与电能之间可以相互转化,以Fe、Cu、C(石墨)、CuSO4溶液、FeSO4溶液、Fe2(SO4)3溶液 、AgNO3溶液为原料,通过原电池反应实现2Fe3+ + Cu=2Fe2+ + Cu2+,请你把下图补充完整,使之形成闭合回路,并用元素符号标明电极。甲池中电解液是 溶液;乙池中电解液是 溶液。(要求:甲、乙两池中电解质元素种类始终保持不变)
(3)某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
①对PM2.5空气样本用蒸馏水处理,制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/ mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
 2NO(g)
2NO(g) 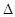 H>0
H>0查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com