
| A�� | pH=2��HA��Һ��pH=12��MOH��Һ����Ȼ�ϣ�c��H+��+c��M+��=c��OH-��+c��A-�� | |
| B�� | B��ˮ�������Ϻ���Һ�����ԣ���Һ�п��ܴ��ڣ�c��NH4+����c��Cl-�� | |
| C�� | ��һ���¶��£���ͬpH���������������Һ��ˮ���������c��H+���ֱ���1.0��0��10-amol/L����1.0��10-bmol/L���ڴ��¶�ʱ��ˮ�����ӻ�Ϊ1.0��10-��a+b�� | |
| D�� | �����£�0.1mol/L��HA pH=3��0.1mol/L ��BOH pH=13������BA��Һ��pH��7 |
���� A���κε������Һ�ж����ڵ���غ㣬���ݵ���غ��жϣ�
B�����ݵ���غ������
C������Kw=c��H+����c��OH-�����㣻
D�������£�0.1 mol/L��HApH=3��˵��HAû����ȫ���룬Ϊ���ᣬ0.1 mol/L ��BOHpH=13��˵��BOH��ȫ���룬Ϊǿ�
��� �⣺A���κε������Һ�ж����ڵ���غ㣬���ݵ���غ��c��H+��+c��M+��=c��OH-��+c��A-������A��ȷ��
B����ˮ�������Ϻ���Һ�����ԣ���Һ�е���غ�Ϊ��c��H+��+c��NH4+��=c��OH-��+c��Cl-���������ԣ�c��H+����c��OH-��������Һ�д��ڣ�c��NH4+����c��Cl-������B����
C��������ˮ���������c��H+��=c��OH-��=1.0��10-amol/L����������Һ��ˮ���������c��H+����1.0��10-bmol/L����������c��H+����1.0��10-bmol/L����Kw=c��H+����c��OH-��=1.0��10-a��1.0��10-b=1.0��10-��a+b������C��ȷ��
D�������£�0.1 mol/L��HApH=3��˵��HAû����ȫ���룬Ϊ���ᣬ0.1 mol/L ��BOHpH=13��˵��BOH��ȫ���룬Ϊǿ���BAΪǿ�������Σ�ˮ��ʼ��ԣ���pH��7����D����
��ѡAC��
���� ���⿼������Ũ�ȴ�С�Ƚϡ��������Һ���йؼ���ȣ���Ŀ�Ѷ��еȣ���ȷ�����Һ��������Լ�����غ��Ӧ���ǽ���Ĺؼ��������ڿ���ѧ���ķ��������ͼ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1ml 1mol/L��NaOH����Һ�еμ�1��2��2mol/LMgCl2��Һ�а�ɫ�������ɣ��ٵμ�2��0.1mol/LFeCl3��Һ�����ֺ��ɫ��������֤��Mg��OH��2��Ksp����Fe��OH��3 | |
| B�� | ��pH=3��CH3COOH��Һ��pH=11��NaOH��Һ�������Ϻ����Һ������ | |
| C�� | ��0.1mol/L��CH3COOH��Һ��0.1mol/L��NaOH��Һ�������Ϻ����Һ������ | |
| D�� | ij���ʵ���Һ����ˮ�������c��H+��=1��10-a mol/L����a��7�������Һ��pHһ��Ϊ14-a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪1-�����ķе�Ϊ117.7�棬����ķе�Ϊ118�棬��ͬѧ����Ũ���������£�ʹ1-�������������������Ӧ�����ᶡ������Ӧ�¶�115��125�棩
��֪1-�����ķе�Ϊ117.7�棬����ķе�Ϊ118�棬��ͬѧ����Ũ���������£�ʹ1-�������������������Ӧ�����ᶡ������Ӧ�¶�115��125�棩�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
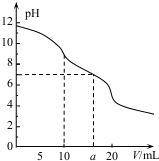 �����£��� 0.1mol•L HCl��Һ�ζ�10.0mLŨ��Ϊ0.1mol•L-1 Na2CO3��Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������
�����£��� 0.1mol•L HCl��Һ�ζ�10.0mLŨ��Ϊ0.1mol•L-1 Na2CO3��Һ�����õζ�������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��V=0ʱ��c��H+��+c��H2CO3��+c��HCO3-��=c��OH-�� | |
| B�� | ��V=5ʱ��c��Na+ ����c��HCO3-����c��CO32- ����c��Cl- �� | |
| C�� | ��V=aʱ��c��Na +����c��Cl- ����c��H+ ��=c��OH- �� | |
| D�� | ��V=10ʱ��c��H+ ��+c��H2CO3��=c��OH- ��+c��CO32-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 12�� | C�� | 15�� | D�� | 20�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
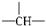 ��a��CH 3������ΪOH��������ʷ�����OH�ĸ�������Ϊ��������
��a��CH 3������ΪOH��������ʷ�����OH�ĸ�������Ϊ��������| A�� | m-a | B�� | n+m+a | C�� | m+1-a | D�� | m+2-a |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com