
【题目】下列有关燃料的说法错误的是
A.燃料燃烧产物CO2是温室气体之一
B.化石燃料完全燃烧不会造成大气污染
C.以液化石油气代替燃油可减少大气污染
D.燃料不完全燃烧排放的CO是大气污染物之一
科目:高中化学 来源: 题型:
【题目】两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中满足上述关系的元素共有
A. 1对 B. 2对 C. 3对 D. 4对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里从海藻中提取碘的流程图如下:

(1)指出制取碘的过程中有关的实验操作名称:
①________________,②____________________。
(2)灼烧海藻时,除需要三脚架外,还需要用到的仪器是 (从下列仪器中选择所需的仪器,将标号字母填写在空白处)。
A烧杯 B坩埚 C表面皿 D泥三角 E酒精灯 F干燥器
(3)提取碘的过程中,可供选择的有机溶剂是_____ ___(填字母序号)。(乙酸、甘油均可溶于水)
A.甲苯、酒精 B.四氯化碳、苯 C.汽油、乙酸 D.汽油、甘油
(4)进行上述蒸馏操作时,最后晶体碘在 里聚集。
(5)含碘的有机物溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察下列实验装置,指出有其错误
有 处。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2; 2NO2+Na2O2=2NaNO3
设计制备装置如下(夹持装置略去):
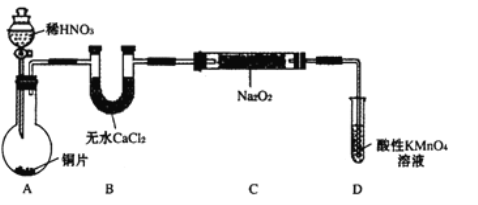
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为 。
(2)如果没有B装置,C中发生的副反应有 , 。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是在A与B装置间增加了 装置,改进后提高了NaNO2的纯度。
【实验Ⅱ】测定制取的样品中NaNO2的含量
步骤:
a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
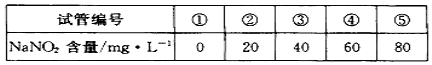
b.称量0.10 g制得的样品溶于水配成500 mL溶液。取5 mL待测液,加入1 mL M溶液,后加蒸馏水至10 mL振荡,与标准色阶比较。
(4)步骤b中比较结果是:待测液颜色与③号色阶相同。则甲同学制得的样品中NaNO2的质量分数是 %。
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
实验方案 | 实验现象 | 实验结论 |
取5mL待测液加入 ,振荡,再加入1ml M溶液 , ,再振荡,与③号色阶对比。 | 维生素C可以有效降低NaNO2 的含量。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯(C7H8)和甘油(C3H8O3)组成的混合物中,若碳元素的质量分数为60%,那么可以推断氢元素的质量分数约为
A.5% B.8.7% C.17.4% D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出此化学反应方程式 。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液的变质情况。
限选试剂为:98%浓硫酸、1%品红溶液、1.0 mol·L-1 KI-淀粉溶液、1.0 mol·L-1NaOH、
澄清石灰水、饱和NaCl溶液
请完成下列探究实验方案。
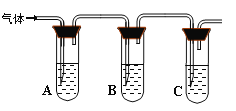
所加试剂 | 预期现象和结论 |
试管A中加足量① ; 试管B中加1%品红溶液; 试管C中加② 。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊。则消毒液部分变质; ③ 则消毒液未变质; ④ 则消毒液完全变质。 |
(3)用滴定法测定消毒液中NaClO的浓度。实验步骤如下:
① 量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液b mL;
② 滴定分析。将c mol·L-1的酸性KMnO4溶液装入 (填酸式或碱式)滴定管中;KMnO4和剩余的Na2SO3发生反应。当溶液由无色变成浅红色,且保持半分钟内红色不褪时,停止滴定,记录数据。重复滴定实验2次,平均消耗酸性KMnO4溶液v mL;
滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4;
2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O
③ 计算消毒液中NaClO的浓度为 mol·L-1(用含a、b、c、v的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氢气的燃烧热为△H=-285.5kJmol-1,则电解水的热化学方程式为2H2O (l)![]() 2H2(g)+O2(g) △H=+285.5kJmol-1
2H2(g)+O2(g) △H=+285.5kJmol-1
B.反应SO2(g)+2H2S(g)=3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g)△H=-38.6kJmol-1
2NH3(g)△H=-38.6kJmol-1
D.由C(石墨,s)=C(金刚石,s)△H=+1.90kJmol-1可知,金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产,回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇,写出相应反应的化学方程式 。
(2)已知:
甲醇脱水反应 2CH3OH(g)═CH3OCH3(g) + H2O(g)△H1=﹣23.9kJmol﹣1
甲醇制烯烃反应 2CH3OH(g)═C2H4(g) + 2H2O(g)△H2=﹣29.1kJmol﹣1
乙醇异构化反应 C2H5OH(g)═CH3OCH3(g)△H3=" +" 50.7kJmol﹣1
则乙烯气相直接水合反应C2H4(g) + H2O(g)═C2H5OH(g)的△H= kJmol﹣1,与间接水合法相比,气相直接水合法的优点是 ;
(3)气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中![]() :
:![]() =1:1)
=1:1)
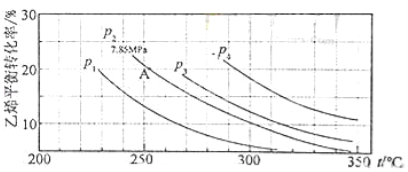
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp= 。
(A点总压为7.85MPa,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);
②图中压强(P1,P2,P3,P4)大小顺序为 ,理由是 ;
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa,![]() :
:![]() =0.6:1,乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 、 。
=0.6:1,乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 、 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com