
【题目】(1)写出下列基团(或官能团)的名称或结构简式:—CH2CH3_____________、—COOR_____________、碳碳双键_____________、醛基_____________。
(2)按系统命名法命名有机物CH3CH(C2H5)CH(CH3)2_____________,![]() _____________
_____________
(3)写出下列各种有机物的结构简式
①2,3-二甲基-4-乙基已烷_____________
②支链只有一个乙基且相对分子质量最小的烷烃_____________
③异戊烷(写出键线式)_____________
【答案】乙基 酯基 >C=C< -CHO或![]() 2,3-二甲基戊烷 己二酸或1,6-己二酸
2,3-二甲基戊烷 己二酸或1,6-己二酸 ![]()
![]()
![]()
【解析】
(1)—CH2CH3为乙基,—COOR为酯基,碳碳双键的结构简式为:>C=C<,醛基的结构简式为:-CHO或![]() ,故答案为:乙基;酯基;>C=C<;-CHO或
,故答案为:乙基;酯基;>C=C<;-CHO或![]() ;
;
(2) CH3CH(C2H5)CH(CH3)2为2,3-二甲基戊烷,![]() 为己二酸或1,6-己二酸,故答案为:2,3-二甲基戊烷;己二酸或1,6-己二酸;
为己二酸或1,6-己二酸,故答案为:2,3-二甲基戊烷;己二酸或1,6-己二酸;
(3) ①2,3-二甲基-4-乙基已烷的结构简式为:![]() ,故答案为:
,故答案为:![]() ;
;
②支链有乙基的烷烃,主链最少为5个C,故支链只有一个乙基且相对分子质量最小的烷烃结构简式为:![]() ,故答案为:
,故答案为:![]() ;
;
③异戊烷的键线式为:![]() ,故答案为:
,故答案为:![]() 。
。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】(1)①CH3COONa溶液呈碱性,原因是____________________(用化学用语表达)。
②在CH3COONa溶液中,各个离子浓度大小关系为_________________________
③写出碳酸钠溶液中电荷守恒关系式_________________________________________
(2)已知:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol。
CO(g)+H2(g) △H=+131.3kJ/mol。
①该反应是________(填“吸热”或“放热”)反应。
②它若反应消耗24gC(s),则反应吸收的热量为___________。
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生反应CO(g)+H2O(g)![]() CO2(g)+H2(g),得到下表中数据:
CO2(g)+H2(g),得到下表中数据:
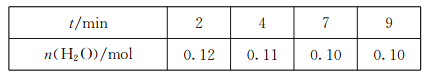
①2min内,v(CO)=________。
②该温度下,此反应的平衡常数的值是________。
③其他条件不变,再充入0.1molCO和0.molH2O(g),达到平衡时CO的体积分数_____(填“增大”“减小”或“不变”)。
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极。请回答下列问题:
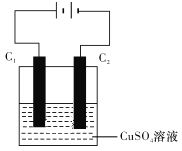
①C1作______(填“阳极”或“阴极”)。
②C2电极的电极反应式为___________。
③惰性电极电解CuSO4溶液的化学方程式是_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
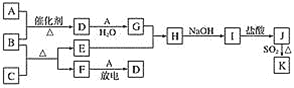
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是( )
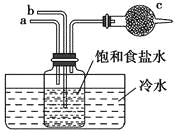
A. a通入CO2,然后b通入NH3,c中放碱石灰
B. b通入NH3,然后a通入CO2,c中放碱石灰
C. a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
D. b通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容积为1L的密闭容器中通入1mol CO2和3mol H2,发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0。下列有关说法正确的是
A. 该反应在高温下才能自发进行
B. 再加入一定量CO2,则n(CH3OH)/n(CO2)减小
C. 温度升高,反应的平衡常数K增大
D. 当CO2和H2转化率相等时,该反应达到化学平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molM和2 molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g)![]() P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )

A. 若X、Y两点的平衡常数分别为K1、K2,则K1>K2
B. 温度为T1时,N的平衡转化率为80%,平衡常数K=40
C. 无论温度为T1还是T2,当容器中气体密度和压强不变时,反应达平衡状态
D. 降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2mol A和1mol B气体加入体积为1L的密闭容器中,发生反应2A(g)+B(g) = 2C(g),若经2秒后测得C的浓度为0.6mol·L-1,现有下列几种说法,其中正确的是 ( )
①用物质A表示的反应平均速率为0.3mol·L-1·S-1
②用物质B表示的反应的平均速率为0.6mol·L-1·S-1
③2 s时物质A的转化率为30%
④2 s时物质B的浓度为0.7mol·L-1
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.将少量SO2气体通入过量氨水中:SO2+NH3·H2O=NH![]() +HSO
+HSO![]()
B.铝溶于NaOH溶液中:2Al+2OH-+2H2O=2AlO![]() +3H2↑
+3H2↑
C.用醋酸除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.用KIO3氧化酸性溶液中的KI:5I-+IO![]() +3H2O=3I2+6OH-
+3H2O=3I2+6OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图所示。若上端开口关闭,可得到强还原性的H·(氢原子);若上端开口打开,并鼓入空气,可得到强氧化性的·OH(羟基自由基)。下列说法错误的是

A. 无论是否鼓入空气,负极的电极反应式均为Fe-2e—===Fe2+
B. 不鼓入空气时,正极的电极反应式为H++e—===H·
C. 鼓入空气时,每生成1mol·OH有2 mol电子发生转移
D. 处理含有草酸(H2C2O4)的污水时,上端开口应打开并鼓入空气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com