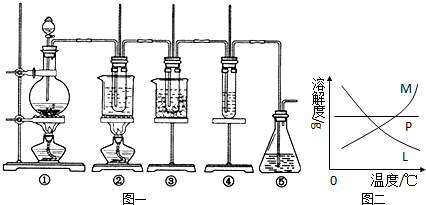
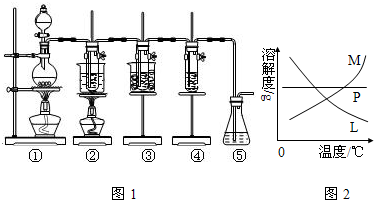
��ʵ�����������ͼ1��ʾװ����ȡ����ء��������ƺ�̽����ˮ�����ʣ�
ͼ1�У���Ϊ��������װ�ã��ڵ��Թ���ʢ��15mL 30% KOH��Һ��������ˮԡ�У��۵��Թ���ʢ��15mL 8% NaOH��Һ�������ڱ�ˮԡ�У��ܵ��Թ��������ɫʯ����Һ����Ϊβ������װ�ã�����д���пհף�
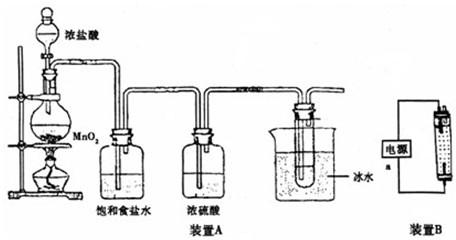
��1��װ�â�����������װ�ã�������ƿ��ʢ��MnO
2���壬�䷴Ӧ�Ļ�ѧ����ʽΪ
MnO
2+4HCl��Ũ��
MnCl
2+Cl
2��+2H
2O
MnO
2+4HCl��Ũ��
MnCl
2+Cl
2��+2H
2O
��
��2�����ʵ������MnO
2�����ˣ����������ʿ��ܿ�����������MnO
2��Cl
2���ǣ�
A��C
A��C
������֪������ǿ��˳��Ϊ��NaBiO
3��PbO
2��MnO
2��Na
2O
2��FeCl
3��
A��NaBiO
3 B��FeCl
3 C��PbO
2 D��Na
2O
2��3���Ƚ���ȡ����غʹ������Ƶ����������ߵIJ����ǣ���
��ȡ�¶Ȳ�ͬ
��ȡ�¶Ȳ�ͬ
�� ��
��ȡʱ���Ũ��Ҳ��ͬ
��ȡʱ���Ũ��Ҳ��ͬ
��
��4����Ӧ��Ͼ���ȴ�ڵ��Թ����д���������������ͼ2�з��ϸþ����ܽ�����ߵ���
M
M
����д�����ĸ�����Ӣڵ��Թ��з�����þ���ķ�����
����
����
����дʵ��������ƣ���
��5�����ݢܵ��Թ�����ɫʯ����Һ����ɫ�仯�ɷ�֤��������ǿ������
����
����
��Ϊʲô��
ʯ����Һ��ɫ������ΪHClO��ǿ�����Զ�����Cl2
ʯ����Һ��ɫ������ΪHClO��ǿ�����Զ�����Cl2
��
��6�����ڵ��Թ���Һ�в�����KClO
3���ɻ���KClO���ɣ��Ҷ��ߵ����ʵ���֮��Ϊ1��2����÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ��
7��3
7��3
��