
【题目】右图是一种试验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
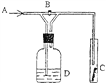
A. 浓H2SO4 B. 浓NaOH溶液
C. 饱和Na2SO4溶液 D. 石灰乳
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】科学家在研究生物体的化学成分时,发现组成生物体的元素在非生物界中也都存在,这一事实主要说明:( )
A. 生物与非生物没有区别
B. 生物来源于非生物
C. 生物界与非生物界具有差异性
D. 生物界与非生物界具有统一性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、纳米技术制成的金属燃料、非金属固体燃料已应用到社会生活和高科技领域.
(1)已知短周期金属元素A和B,其单质单位质量的燃烧热大,可用作燃料.其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 899.5 | 1757.1 | 14848.7 | 21006.6 |
B | 738 | 1451 | 7733 | 10540 |
①根据上述数据分析,B在周期表中位于区,其最高价应为;
②若某同学将B原子的基态外围电子排布式写成了ns1np1 , 违反了原理;
③B元素的第一电离能大于Al,原因是;
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.①已知金刚石中的C﹣C的键长为154.45pm,C60中C﹣C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 .
②C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子相对稳定结构,则C60分子中σ键与π键的数目之比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)Ⅰ.某同学为了验证氢气还原氧化铜的反应产物,设计了如图1所示的实验装置.
①写出编号仪器的名称:①② .
②浓硫酸的作用是 .
③本实验需要加热的装置为(填字母编号).
④写出装置C、D中可观察到的现象:C , D .
⑤D中反应每生成1mol水分子,转移的电子数为个.
(2)Ⅱ.实验时他需要1.0mol/L的硫酸溶液250mL.根据溶液的配制回答下列问题.①在如图2所示仪器中,配制上述溶液肯定不需要的是(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 .
②在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转几次,摇匀.
③根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL,如果实验室有15mL、20mL、50mL量筒,应选用mL量筒最好.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.已知:氧化性:IO3﹣>Fe3+>I2;还原性:S2O ![]() >I﹣
>I﹣
3I2+6OH﹣=IO3﹣+5I﹣+3H2O;KI+I2═KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得试液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.①加KSCN溶液后显红色,该红色物质是(用化学式表示);CCl4中显紫红色的物质是(用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为、 .
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境下KI与氧气反应的化学方程式: .
将I2溶于KI溶液,在低温条件下,可制得KI3H2O.该物质作为食盐加碘剂是否合适?(填“是”或“否”),并说明理由 .
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是 . A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取溴苯的三个装置,根据要求回答下列各题: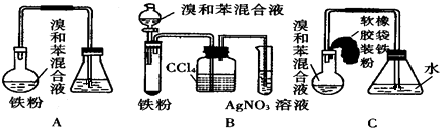
(1)装置A烧瓶中发生反应的化学方程式是;装置A中左侧长导管的作用是;装置A和C中的两处明显错误是、 .
(2)在按装置B、C装好仪器及药品后要使反应开始,应对装置B进行的操作是 , 应对装置C进行的操作是
(3)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作.A装置中这一问题在实验中造成的后果是 .
(4)B中采用了洗气瓶吸收装置,其作用是 . 反应后洗气瓶中可能出现的现象是 .
(5)B装置也存在两个明显的缺点,其中之一与A、C中的错误相同,而另一个缺点是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:

(1)写出三种试剂的化学式:A________,B________,C________。
(2)加过量A的原因是:________________________________________________,
有关反应的化学方程式为:___________________、_____________________。
(3)加过量B的原因是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
(1)甲组同学采用如右图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2g铜。
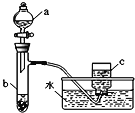
①请写出铜与稀硝酸反应的离子反应方程式_________________________________________。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有__________________________。
③仪器c中收集的气体主要是_______________________。(填分子式)
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是______g。
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+。
①反应结束后的溶液中NO3-的物质的量的取值范围是___________(用含a的代数式等表示)
②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+)∶n(Fe2+)为3∶1,则b∶a的值为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com