
0.6 mol/L的Fe2(SO4)3 和1.2 mol/L的CuSO4 的混合溶液200 mL,加入一定量铁粉充分反应后,测得溶液中Fe2+ 与Cu2+ 物质的量之比为2∶1,则加入铁粉的物质的量为
A.0.16mol B.0.22mol C.0.30mol D.0.48mol
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:选择题
下列措施是为了降低化学反应速率的是
A.食品放在冰箱中贮藏
B.用铁粉代替铁钉与稀硫酸反应制取氢气
C.合成氨工业中使用催化剂
D.在试管中进行铝和盐酸反应时,稍微加热
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
下列实验操作中错误的是
A.蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.过滤操作时,向过滤器中倾倒液体时一定要用玻璃棒引流
D.由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三第一阶段考试理综化学试卷(解析版) 题型:实验题
(14分)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验 小组通过
小组通过 实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4, Cu2O在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂.
(1)若假设1成立,则实验现象是_________。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?___________。
(3)若固体粉末完全溶解无固体存在,滴加 KSCN 试剂时溶液不变红色,则证明原固体粉末是________,写出发生反应的离子方程式________。
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为________________。
(5)欲利用红色粉末Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4?5H2O),经查阅资料得知,在溶液中调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 6.0 | 7.5 | 1.4 |
沉淀完全pH[来: | 13 | 14 | 3.7 |
实验室有下列试剂可供选择:
A.氯水
B.H2O2
C.硝酸
D.NaOH
E.氨水
F.Cu2(OH)2CO3
实验小组设计如下实验方案:
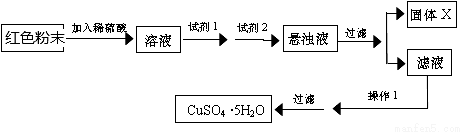
试回答:①试剂I为____________,试剂II为_____________(填字母)。
②固体X的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是

A.OA段所发生反应的离子方程式: H++OH-==H2O;CO32- +H+ ==HCO
B.NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1
C.产生的CO2体积(标准状况下)为0.056 L
D.原NaOH溶液的物质的量浓度为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是
A.FeCl2溶液(FeCl3):Fe粉 B.CO2 (SO2):饱和的Na2CO3溶液
C.Al2O3 (SiO2):NaOH溶液 D.NaHCO3溶液(Na2CO3):Ca(OH)2溶液
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:实验题
(13分)I.高锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制
备高锰酸钾,其部分流程如下:

(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是 (用化学程式表示)。
(2)第④步通人适量CO2,发生反应生成Mn04和Mn02和碳酸盐,则发生反应的离子方程式为___ _。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是 (用化学方程式表示)。
(4)H2O2和KMn04都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,写出该反应的离子方程式:_____ 。
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质。

(5)若从左端分别通人SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);
(6)若装置B中装有5.0 mL l.0 mol/L的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2 mol电子,该反应的化学方程式为 。
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式__ __。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:选择题
如图是草酸溶液中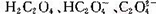 三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下到有关说法不正确的是
三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下到有关说法不正确的是
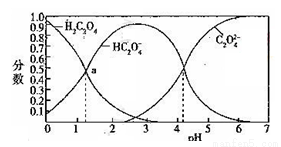
A.pH=5的溶液中: 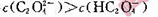
B.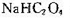 溶液中:
溶液中: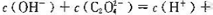
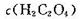
C.向  溶液中加强酸至pH与a点对应时,溶液中
溶液中加强酸至pH与a点对应时,溶液中 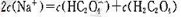
D.为使溶液中c( 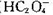 )尽可能多一些,溶液的pH最好控制在2.7左右
)尽可能多一些,溶液的pH最好控制在2.7左右
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a—的电子层结构与氦相同,b和c的次外层有8个电子,c—和d+的电子层结构相同。下列叙述错误的是
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com