
家用食醋的主要成分是醋酸(CH3COOH),它的官能团是
A.-COOH B.-CH3 C.-OH D.-H
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:2014-2015湖南省娄底市名校高一上学期期末化学试卷(解析版) 题型:填空题
(10分)现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是 ,遇KSCN溶液显血红色的是 ,加铁粉后溶液增重的是 ;
(2)向③的溶液中滴加NaOH溶液,现象是 ,写出此步操作属于氧化还原反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市名校高二上学期期末化学(理)试卷(解析版) 题型:填空题
(10分)以下是某实验小组用工业硫酸铜(含硫酸亚铁等杂质)进行提纯实验,得到纯净硫酸铜晶体的流程:(已知数据:lg2=0.3;lg5=0.7)

请回答下列问题:
(1)①步骤I的目的是除不溶性杂质。操作是 。
②步骤Ⅱ是为了除去Fe2+,常加入氧化剂使Fe2+氧化为Fe3+,下列物质最适合的是________。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________。
A.NaOH B.NH3·H2O C.CuO D.Cu
(2)已知常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,分别写出Cu(OH)2开始沉淀时溶液的pH=________并写出步骤Ⅱ调节溶液pH的合理范围______。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市名校高二上学期期末化学(理)试卷(解析版) 题型:选择题
下列说法中,正确的是
A.某离子被沉淀完全是指该离子在溶液中的浓度变为0
B.某物质的溶解性为难溶,则该物质的溶解度为0
C.一般来说,溶解度小的难溶物容易转化为溶解度大的难溶物
D.沉淀的生成、溶解和转化其实质都是沉淀发生了溶解平衡的移动
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(文)试卷(解析版) 题型:填空题
(8分)现有:①铁锅 ②鸡蛋 ③白酒 ④乙烯。根据所学知识,请你在上述四种物质中选择合适的物质填入下列空格中(填编号)。
(1)可以作为水果催熟剂的是 ;
(2)含有乙醇的是 ;
(3)在潮湿的空气中会生锈的是 ;
(4)富含蛋白质的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
下列关于液氯的说法中,不正确的是
A.液氯属于混合物
B.液氯呈黄绿色
C.液氯是一种有色、有味、有毒的液体
D.液氯能使湿润的红色布条褪色
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高二上学期期末考试化学(文)试卷(解析版) 题型:选择题
下列物质中,含有共价键的化合物是
A.H2 B.Al C.KI D.CO2
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省娄底市高一上学期期末考试化学试卷(解析版) 题型:选择题
光纤通信是一种现代化的通信手段,制造光纤的主要原料是
A.CaCO3 B.CaO C.Na2CO3 D.SiO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省清远市高三上学期期末理综化学试卷(解析版) 题型:填空题
(16分)随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%,CO2的排放量也要大幅减少。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) △H1=-574kJ·mol-1
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H2
③CH4(g) + 2NO2 (g) = N2(g) + CO2(g) + 2H2O(g) △H3=-867kJ·mol-1
则△H2 = 。
Ⅱ.化石燃料的燃烧、含硫金属矿石的冶炼和硫酸的生产过程中产生的SO2是大气中SO2的主要来源。
(1)将煤转化为水煤气是将煤转化为洁净燃料的方法之一,反应为C(s) + H2O(g)  CO(g) + H2(g)
CO(g) + H2(g)
①该反应的化学平衡常数表达式为:K= 。
②800℃时,将1molCO、3mol H2O、1mol H2充入容积为1L的容器中,发生反应: CO(g) + H2O(g)  CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为_________,800℃时该反应的平衡常数为_________。
CO2(g) + H2(g),一定时间后达到平衡时,测得容器中CO2浓度为0.5mol·L-1,则CO的转化率为_________,800℃时该反应的平衡常数为_________。
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应_______________________________________。
②用化学平衡移动的原理分析,在 HI分解反应中使用膜反应器分离出H2的目的是: ___________。
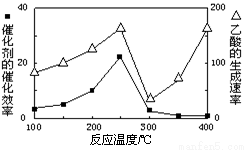
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g) CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
CH3COOH(g)直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
如图所示。由下图可以得出的结论是(写两条):_____________________、___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com