
某元素构成的双原子单质分子有三种,其式量分别为158,160,162.在天然单质中,此三种单质的物质的量之比为1∶1∶1,由此推断以下结论中,正确的是
[ ]
A.此元素有三种同位素
B.其中一种同位素质量数为80
C.其中质量数为79的同位素原子占原子总数的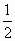
D.此元素单质的平均式量为160
|
【巧解导析】若元素有两种同位素aX,bX,则构成的双原子单质分子有aXaX,aXbX,bXbX三种.若a<b,则2a=158,2b=162,求得两种同位素的质量数分别为79和81.由三种单质的物质的量之比为1∶1∶1,可求得aX,bX的原子个数比(设物质的量为x,则aX∶bX= |
|
【巧解点悟】解题的关键是正确判断同位素的种类数.本题很容易不加分析地认为有三种X2分子即说明X有三种同位素而出错. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A.CH8N4 B.C6H12N4 C.C6H10N4 D.C4H8N4?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com