
(10分)![]()
 铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
![]()
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为__________
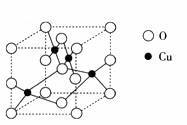
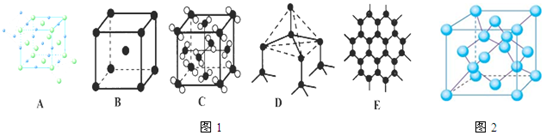
(2) 右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为_________。
(3)胆矾CuSO4?5H2O可写成[Cu(H2O4)]SO4 ?H2O,其结构示意图如下:
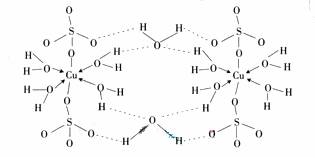
下列说法正确的是__________(填字母)。
A. 在上述结构示意图中,所有氧原子都采用sp3杂化
B. 在上述结构示意图中,存在配位键、共价键和离子键
C. 胆矾是分子晶体,分子间存在氢键
D. 胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______________。
(5)Cu2O的熔点比Cu2S的_________(填“高”或“低”),请解释原因__________。
(1)[Ar]3d9或1s22s22p63s23p63d9
(2)4个
(3)B、D
(4)N、F、H三种元素的电负性:F>N>H,在NF3中,共用电子对偏向F,偏离N原子使得氮原子上的孤对电子难于与Cu2+形成配位键。
(5)高 。Cu2O与Cu2S相比阳离子相同,阴离子所带的电荷数也相同,但O2-半径比S2-半径小,所以Cu2O的晶格能更大,熔点更高。
解析:
(1)Cu(电子排布式为:[Ar]3d104s1)![]() Cu2+的过程中,参与反应的电子是最外层的4s及3d上各一个电子,故Cu2+离子的电子是为:[Ar]3d9或1s22s22p63s23p63d9;
Cu2+的过程中,参与反应的电子是最外层的4s及3d上各一个电子,故Cu2+离子的电子是为:[Ar]3d9或1s22s22p63s23p63d9;
(2)从图中可以看出阴离子在晶胞有四类:顶点(8个)、棱上(4个)、面上(2个)、体心(1个),根据立方体的分摊法,可知该晶胞中有4个阴离子;
(3)胆矾是由水合铜离子及硫酸根离子构成的,属于离子化合物,C不正确;
(4)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子;
(5)由于氧离子的例子半径小于硫离子的离子半径,所以亚铜离子与氧离子形成的离子键强于亚铜离子与硫离子形成的离子键,所以Cu2O的熔点比Cu2S的高。


科目:高中化学 来源: 题型:阅读理解
 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.| 2880 |
| NA |
| 2880 |
| NA |
| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都七中高二(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省雅安中学高二(上)月考化学试卷(10月份)(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com