

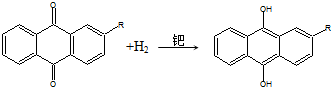
| A. | H2O2可用作漂白剂、消毒剂,也可作为火箭燃料 | |
| B. | H2O2可使湿润的KI淀粉试纸变蓝 | |
| C. | 蒽醌氧化法生产H2O2的实际结果是H2和O2生成H2O2 | |
| D. | H2O2化学性质稳定,便于储存和运输 |
分析 过氧化氢含有过氧键,具有强氧化性,可作漂白剂、消毒剂,对比两步反应可知,两步反应相加为H2+O2=H2O2,反应前后乙基蒽醌不变,应为该反应的催化剂,以此解答该题.
解答 解:A.过氧化氢含有过氧键,具有强氧化性,可作漂白剂、消毒剂,故A不选;
B.过氧化氢具有强氧化性,可氧化KI生成碘,使淀粉变蓝色,故B不选;
C.对比两步反应可知,两步反应相加为H2+O2=H2O2,反应前后乙基蒽醌不变,应为该反应的催化剂,故C不选;
D.过氧化氢具有强氧化性,易与还原性物质反应,催化条件下易分解,故D选.
故选D.
点评 本题考查有机合成反应原理的探讨,题目难度不大,本题注意把握反应机理的探讨,注意催化剂的性质,把握绿色化学的定义.


科目:高中化学 来源: 题型:解答题
 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S通入CuSO4溶液中 S2-+Cu2+=CuS↓ | |
| B. | AgCl投入KI溶液中 Ag++I-=AgI↓ | |
| C. | Na2S的水解反应 S2-+2H2O?H2S+2OH- | |
| D. | NH4NO3溶液呈酸性 NH4++H2O?NH3•H2O+H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 半径:Li>Na>K>Rb | |
| B. | 酸性:HClO4>H2SO4>H3PO4>H2CO3 | |
| C. | 气态氢化物的稳定性:HI>HBr>HCl>HF | |
| D. | 还原性:Cl->Br->I->S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O | B. | CaO(s) | C. | CaCO3 (s) | D. | NaOH (s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
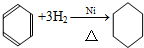 ;
; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com