
| A. | 用10 mL 量筒量取5.25 mL盐酸 | |
| B. | 用广泛pH试纸测得某溶液的pH值为12.5 | |
| C. | 用托盘天平称取25.12g NaCl固体 | |
| D. | 配制70mL 0.1 mol/L的稀硫酸选用100 mL容量瓶 |
分析 A.量筒的感量是0.1mL;
B.广泛pH试纸的测定值是整数;
C.托盘天平的感量是0.1g;
D.配制一定物质的量浓度溶液时选取容量瓶的规格应该等于或稍微大于配制溶液体积.
解答 解:A.量筒的感量是0.1mL,所以不能用10 mL 量筒量取5.25 mL盐酸,故A错误;
B.广泛pH试纸的测定值是整数,所以不能用广泛pH试纸测得某溶液的pH值为12.5,故B错误;
C.托盘天平的感量是0.1g,所以不能用托盘天平称取25.12g NaCl固体,故C错误;
D.配制一定物质的量浓度溶液时选取容量瓶的规格应该等于或稍微大于配制溶液体积,实验室没有70mL容量瓶,有100mL容量瓶,所以应该选取100mL容量瓶,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器的选取和仪器的使用,明确仪器用途及其使用方法是解本题关键,知道滴定管、量筒、托盘天平的感量,知道容量瓶、量筒的选取方法,易错选项是D.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| B. | 氢氧燃料电池正极消耗 22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 欲配制1.00L 1.00mol.L-1的NaCl溶液,可将 58.5gNaCl溶于 1.00L水中 | |
| D. | 10LpH=13的NaOH溶液中含有的OH-离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 臭氧层中氧分解历程如图所示,下列说法正确的是( )
臭氧层中氧分解历程如图所示,下列说法正确的是( )| A. | 催化反应①②均为放热反应 | |
| B. | 催化剂不能改变该反应的反应热 | |
| C. | ClO是该反应的催化剂 | |
| D. | 在该反应过程中没有化学键的断裂与生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
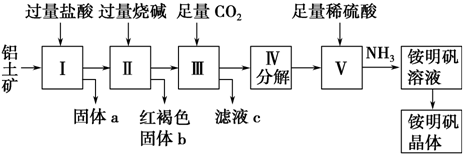
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ | |
| B. | 在pH=12的溶液中:ClO-、SO32-、Na+、K+ | |
| C. | 能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COOO-、I- | |
| D. | 澄清透明的溶液中:Cu2+、Fe3+、NO3?、Cl ? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 下列各组物质中,物质之间通过一步反应就能实现图所示转化的是
下列各组物质中,物质之间通过一步反应就能实现图所示转化的是| 编号 | a | b | c | d |
| ① | Na2O | Na2O2 | Na | NaOH |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| ③ | FeCl2 | FeC13 | Fe | CuCl2 |
| ④ | NO | NO2 | N2 | HNO3 |
| A. | ②③ | B. | ③④ | C. | ①②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| M | Y | |
| Z | N |
| A. | 元素Y与元素Z的最高正化合价之和的数值等于13 | |
| B. | 元素Z的含氧酸的酸性比元素N的强 | |
| C. | 离子半径的大小顺序为Z(n+1)->M(n+1)->Yn- | |
| D. | Z的气态氢化物的还原性和热稳定性均比N强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com