
| A. | ① | B. | ①② | C. | ②③ | D. | ④⑤ |
分析 ①根据碳酸钠、碳酸氢钠的性质、用途判断;
②能和水反应只生成碱的氧化物是碱性氧化物;
③某溶液焰色反应时,如果透过蓝色钴玻璃火焰呈紫色,说明该溶液中含有钾元素;
④Na2CO3和Ca(OH)2混合后生成CaCO3,发生Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,NaHCO3可与澄清石灰水发生Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O或Ca(OH)2+2NaHCO3═CaCO3↓+Na2CO3+2H2O,Na2CO3与NaOH不反应;
⑤若Na2CO3溶液中混有NaHCO3,可向溶液中加入氢氧化钠,碳酸氢钠的溶解度小于碳酸钠的溶解度.
解答 解:①碳酸钠可用于制备硅酸钠、硬质酸钠等,可用于制玻璃、肥皂、造纸、纺织等工业,NaHCO3不稳定,碱性较弱,可与酸反应,可用于治胃酸过多,制发酵粉等,故①正确;
②Na2O和水反应只生成碱,非氧化还原反应,氧化钠是碱性氧化物,Na2O2和水反应生成氢氧化钠和氧气,不是碱性氧化物,故②错误;
③某溶液焰色反应时,如果透过蓝色钴玻璃火焰呈紫色,说明该溶液中含有钾元素,故③错误;
④Na2CO3和Ca(OH)2混合后生成CaCO3,发生Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,NaHCO3可与澄清石灰水发生Ca(OH)2+NaHCO3═CaCO3↓+NaOH+H2O或Ca(OH)2+2NaHCO3═CaCO3↓+Na2CO3+2H2O,Na2CO3与NaOH不反应,故④错误;
⑤若Na2CO3溶液中混有NaHCO3,可向溶液中加入氢氧化钠,而不是通入二氧化碳气体,碳酸氢钠的溶解度小于碳酸钠的溶解度,故⑤错误;
故选A.
点评 本题考查碳酸钠与碳酸氢钠的性质,涉及等浓度溶液碱性强弱、溶解度、热稳定性等知识,学习时注意基础知识的对比记忆.


科目:高中化学 来源: 题型:选择题
| A. | 在强碱性溶液中能大量存在:Na+、K+、Cl-、HCO3- | |
| B. | 加入金属铝后溶液中有大量气泡产生的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| C. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| D. | 溶液通入足量氨气后各离子还能大量存在:K+ Na+ AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 216g | B. | 188g | C. | 180g | D. | 148g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl的电子式: | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | Mg原子结构示意图: | |
| D. | 硫酸铁的电离方程式 Fe2(SO4)3=2Fe3++3SO42ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
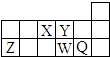
| A. | 离子半径的大小顺序为W>Q>Y>Z | |
| B. | X、Y、W三种元素的非金属性大小顺序为X>Y>W | |
| C. | X、Z、W三种元素的最高价氧化物对应的水化物均能与强碱反应 | |
| D. | 元素X的最简单氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO3>I->Fe2+>NO | B. | I->Fe2+>H2SO3>NO | ||
| C. | Fe2+>I->H2SO3>NO | D. | NO>Fe2+>H2SO3>I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物和生成物均为分子晶体 | |
| B. | 反应物和生成物都为直线型分子 | |
| C. | 反应时旧键断裂放出能量,新键形成吸收能量 | |
| D. | 产物中CO2的键能大于H2O,所以沸点高于H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述 | 判断 |
| A | Si有良好的半导体性能 | 可用于制备光导纤维 |
| B | 苏打受热易分解 | 可用作面包发酵剂 |
| C | 硅胶多孔、吸水能力强 | 可用作袋装食品的干燥剂 |
| D | 干冰升华放出大量的热 | 可用作制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com