
| A. | 苯酚与氢氧化钠溶液反应 | |
| B. | 溴乙烷与NaOH溶液混和共热CH3CH2Br+NaOH$→_{△}^{水}$CH2═CH2↑+H2O+NaBr | |
| C. | 乙醛与银氨溶液反应 CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | 乙醇的消去反应 CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O |
分析 A.苯酚与氢氧化钠反应,反应生成苯酚钠和水;
B.溴乙烷和氢氧化钠醇溶液共热生成乙烯和溴化钠和水,溴乙烷和氢氧化钠水溶液共热生成乙醇和溴化钠;
C.乙醛发生银镜反应,是醛基的还原性,被弱氧化剂氧化为乙酸,发生的是氧化反应;
D.乙醇在浓硫酸作催化剂、加热条件下发生消去反应,羟基和连接烃基碳原子相邻碳上氢原子结合生成水.
解答 解:A.苯酚与氢氧化钠反应,反应生成苯酚钠和水,反应为C6H5OH+NaOH→C6H5ONa+H2O,离子反应为:C6H5OH+OH-→C6H5O-+H2O,故A正确;
B.卤代烃在碱性水溶液加热条件下发生取代反应,由溴乙烷变成乙醇,生成乙醇与溴化钠方程式为:CH3CH2Br+NaOH$\stackrel{△}{→}$CH3CH2OH+NaBr,故B错误;
C.乙醛与银氨溶液反应,醛基被氧化成羧基,反应为:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O,故C正确;
D.乙醇在浓硫酸作催化剂、加热条件下发生消去反应,羟基和连接烃基碳原子相邻碳上氢原子结合生成水,CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,故D正确;
故选B.
点评 本题考查有机物的结构与性质,侧重性质及反应方程式书写的考查,为高频考点,把握官能团的性质为解答的关键,注意卤代烃水解、消去反应条件的异同,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SO2和CO2都是酸性氧化物,SO2与Na2O2反应生成Na2SO3和O2 | |
| B. | 84 g NaHCO3受热分解,将生成的气体通过足量的Na2O2,固体质量增加31 g | |
| C. | 将Na2O2投入到酚酞试液中,溶液变红 | |
| D. | Na2O2与水的反应中,Na2O2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| C | 乙醇(乙酸) | 新制生石灰 | 蒸馏 |
| D | 甲苯(苯酚) | 浓溴水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中不一定含有Na+ | |
| B. | 该溶液中肯定含有NH4+、SO42-、CO32-、NO3- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含Na+,且c(Na+)≥0.1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
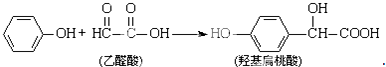
| A. | 该反应是取代反应 | |
| B. | 乙醛酸与H2在热的镍催化下反应生成乙二醇 | |
| C. | 1mol羟基扁桃酸能与3mol NaOH反应 | |
| D. | 1mol羟基扁桃酸能与1mol NaHCO3反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| B. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+3Ag↓+H2O | |
| C. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | |
| D. | 苯酚钠溶于醋酸溶液:C6H5O-+CH3COOH→C6H5OH+CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
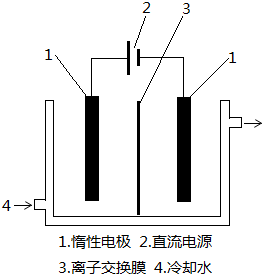
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com