
分析 (1)氢氟酸是一种弱酸,溶液中存在电离平衡,离子方程式用可逆号;
(2)电离平衡常数等于溶液中电离出的离子浓度的幂次方乘积除以平衡状态下分子的浓度;
(3)等物质的量的氢氟酸和氢氧化钠恰好反应生成氟化钠,溶液呈碱性;
解答 解:(1)氢氟酸是一种弱酸,溶液中存在电离平衡,电离方程式为:HF?H++F-,故答案为:HF?H++F-;
(2)电离方程式为:HF?H++F-,氢氟酸的电离平衡常数表达式:K=$\frac{[{H}^{+}][{F}^{-}]}{[HF]}$,故答案为:$\frac{[{H}^{+}][{F}^{-}]}{[HF]}$;
(3)在20mL 0.1mol•L-1氢氟酸中加入V mL pH=13NaOH溶液,当V=20时,氢氟酸和氢氧化钠等物质的量恰好完全反应,HF+NaOH=NaF+H2O,等物质的量反应生成NaF,氟化钠是强碱弱酸盐,溶液显碱性,
故答案为:碱;
点评 本题考查了弱电解质电离平衡,电离方程式,电离平衡常数的理解应用,熟练掌握基础知识是解题关键,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KHSO4═K++H++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Mg(NO3)2═Mg2++(NO3)22- | D. | KClO3═K++Cl5-+3O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
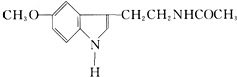
| A. | 它属于芳香族化合物 | B. | 它属于高分子化合物 | ||
| C. | 分子式为C13N2H16O2 | D. | 在一定条件下可以发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2 | B. | HCl | C. | NH3•H2O | D. | CH3COONa |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在FeCl3溶液中加入NaOH溶液 | B. | 加热煮沸FeCl3溶液 | ||
| C. | 把FeCl3溶液滴入沸水中 | D. | 把饱和的FeCl3溶液滴入到沸水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | ||
| C. | 2:1 | D. | 有一装置不消耗水,无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH | B. | H2SO4 | C. | BaCl2 | D. | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 隔膜电解法是一种处理高浓度乙醛废水的新方法,乙醛分别在阴、阳极发生反应转化为乙醇和乙酸.实验室以一定浓度的乙醛-硫酸钠溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法正确的是( )
隔膜电解法是一种处理高浓度乙醛废水的新方法,乙醛分别在阴、阳极发生反应转化为乙醇和乙酸.实验室以一定浓度的乙醛-硫酸钠溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示.下列说法正确的是( )| A. | 若以氢氧燃料电池为直流电源,燃料电池的b极应通入空气 | |
| B. | 电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2 | |
| C. | 阳极反应CH3CHO-2e-+2H+═CH3COOH+H2O | |
| D. | 电解过程中,由于硫酸钠不参与电极反应,故阳极区始终c(Na+)=2 c(SO42-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com