
(13分)如图所示,各物质间有下列转化关系:
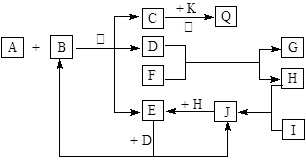
A、F分别为淡黄色固体,A与B的浓溶液反应可以生成C、D、E三种物质,D为无色液体,K为红色金属单质,能在加热条件下与C的浓溶液反应,生成气体Q。I和H为气态双原子分子。反应过程中部分条件和产物均略去。
(1) I的电子式:____________________。
(2) 反应A+ B的化学方程式:_________________________________________________。
(3) 将Q和E按2∶1同时通入品红溶液中,若产物之一含I,则现象可能为___________,原理是(用化学方程式表示)______________________________________________。
(4) 若标准状况下将11.2 L Q通入到500 mL 1.5 mol /L 的G溶液中,请将最终溶液的溶质成分及物质的量填入下表(可不填满)。
| 溶质(化学式) | 物质的量 |
|
|
|
|
|
|
|
|
|
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 ,其核磁共振氢谱中有2个信号(参见图).
,其核磁共振氢谱中有2个信号(参见图).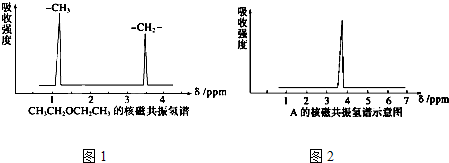
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
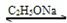 CH3COCH2COOC2H5+C2H5OH
CH3COCH2COOC2H5+C2H5OH| 回流 |
| 振荡② |
| 回收有机液体③ |
| 加入乙酸乙酯④ |
| 乙酸酸化⑤ |
| ⑥ |
| ⑦ |
| 钠 | 苯 | 甲苯 | 对二甲苯 | 四氯化碳 | |
| 密度(g/cm3) | 0.97 | 0.88 | 0.87 | 0.86 | 1.60 |
| 熔点(℃) | 97.8 | 5.5 | -95 | 13.3 | -22.8 |
| 沸点(℃) | 881.4 | 80 | 111 | 138.4 | 76.8 |
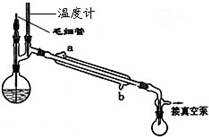
| 无水硫酸钠 |
| 过滤 |
| 水浴蒸馏 |
| 减压蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况,回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
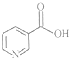 烟酸也称维生素B3,它是人体必需的13种维生素之一,具有促进血液循环、使皮肤更健康、预防和缓解严重的偏头痛等功效.烟酸的结构简式如图所示,下列说法错误的是( )
烟酸也称维生素B3,它是人体必需的13种维生素之一,具有促进血液循环、使皮肤更健康、预防和缓解严重的偏头痛等功效.烟酸的结构简式如图所示,下列说法错误的是( )| A、烟酸能够与苯甲醇发生酯化反应 | B、烟酸能够与氢气发生加成反应 | C、烟酸与硝基苯互为同分异构体 | D、烟酸完全燃烧的产物均为极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 16.
16.
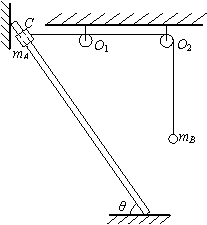
(如东启东期中联考13分)如图所示,一轻绳绕过无摩擦的两个轻质小定滑轮O1、O2和质量mB=m的小球连接,另一端与套在光滑直杆上质量mA=m的小物块连接,已知直杆两端固定,与两定滑轮在同一竖直平面内,与水平面的夹角θ=60°,直杆上C点与两定滑轮均在同一高度,C点到定滑轮O1的距离为L,重力加速度为g,设直杆足够长,小球运动过程中不会与其他物体相碰.现将小物块从C点由静止释放,试求:
(1)小球下降到最低点时,小物块的机械能(取C点所在的水平面为参考平面);
(2)小物块能下滑的最大距离;
(3)小物块在下滑距离为L时的速度大小.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com