
| 1 |
| 2 |
| 1 |
| 2 |
| c(SO32-)c(H+) |
| c(HSO3-) |
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��2KClO3
| ||||
B��2P+5Cl2
| ||||
C��MnO2+4HCl��Ũ��
| ||||
D��H2+Cl2
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ʾ
��ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͬѧ��������茶�������ˮ����ˮ���½���˵�������ˮ�������ȵ� |
| B����ͬѧ���ڴ�����Һ�м���̼����立�ĩ������Һ�¶��½���˵������ˮ�������ȵ� |
| C����ͬѧ���ڴ�������Һ�м�������ƾ��壬����Һ�¶��½���˵������ˮ�������ȵ� |
| D����ͬѧ���ڴ�������Һ�е����̪��Һ�����Ⱥ�����ɫ���˵������ˮ�������ȵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
| B��CH2 CH2Br2 |
C��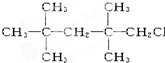 |
| D��CH2ClCH2CH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH3Cl+Cl2��CH2Cl2+HCl | |||
| B��CH2=CH2+HO-H��HOCH2-CH3 | |||
C��CH3COOCH2CH3+H2O
| |||
D�� +Br2 +Br2
 +HBr +HBr |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���ۢ� |
| C���٢ۢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2NH3��g��?3H2��g��+N2��g������H��0 |
| B��3O2��g��?2O3��g������H��0 |
| C��H2��g��+I2��g��?2HI��g������H��0 |
| D��2NO2��g��?N2O4��g������H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʯī�Ƚ��ʯ���ȶ� |
| B��ʯī�ͽ��ʯ�����ת�� |
| C�����ʯ��ʯī���ȶ� |
| D��ʯī�ͽ��ʯ���ܻ���ת�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com