
 某温度下,相同pH值的氨水和氢氧化钠溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )
某温度下,相同pH值的氨水和氢氧化钠溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.据图判断正确的是( )| A、Ⅱ为氨水稀释时的pH值变化曲线 |
| B、a、b、c三点溶液的导电性:c>b=a |
| C、a、b、c三点溶液中水的电离程度:c=b>a |
| D、用相同浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸的体积:Vb=Vc |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
| A、将氯化铁晶体溶解于浓盐酸中配制氯化铁溶液 |
| B、温度升高,水的电离程度增大 |
| C、氯水中加入碳酸钙,漂白性增强 |
| D、反应H2(g)+I2(g)?2HI(g)达平衡后,缩小反应容器体积,混合气体颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
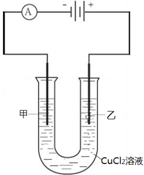
| A、甲电极为阳极 |
| B、阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| C、阴极发生还原反应 |
| D、通电时,溶液中的离子作定向运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.查看答案和解析>>
科目:高中化学 来源: 题型:
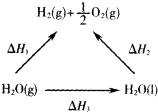
| A、△H1>△H2 |
| B、△H2<△H3 |
| C、△H1=△H2+△H3 |
| D、△H1+△H3>△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com