
分析 微粒中各个字母所表示的含义:X是元素符号,A是质量数,Z是质子数,b是该微粒所含X的个数,n是整个微粒所带的负电荷数,即从外界夺得的电子数.
解答 解:一个X原子所含质子、中子、核外电子的总数为A+Z,则b个X原子所含三种基本微粒之和为(A+Z)×b,再加上从外界夺得的n个电子,得出答案为:(A+Z)×b+n.
需要注意的是:n个负电荷是整个微粒所显示的,而不是由一个X所显示的,所以应该是先用一个X原子的质子、中子、电子数之和乘以X的个数后再加所显示的负电荷,学习者容易将顺序搞错,往往写成(A+Z+n)×b;带负电荷说明微粒从外界得到了电子,在算式中应该用加号,相反,带正电荷说明微粒本身失去了电子,在算式中应该用减号,
答:一个$_Z^AX_b^{n-}$中所含质子、中子、核外电子的总数是(A+Z)×b+n.
点评 本题考查原子构成,塑造了一个元素符号周围有四个角标的完整的典型符号代表,它能引导在更深层次上理解$_Z^AX$的意义以及质子、中子和电子之间的数量关系和电性关系,如果感觉符号比较抽象,可以列举符合要求的一个实例,利用对比的方法加以理解,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
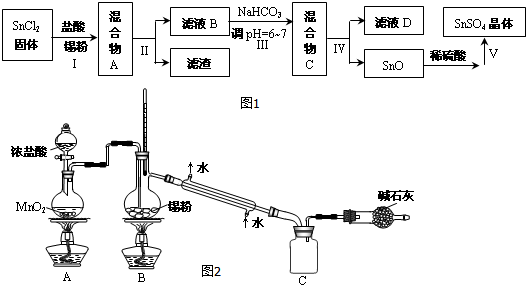
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鱼虾放久了会产生不愉快的腥臭气味,应当用水冲洗,并在烹调时加人少量食醋 | |
| B. | “酸可除锈”“洗涤剂可去油”都是发生了化学变化 | |
| C. | 被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注人人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 煤酚皂溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可以使蛋白质发生变性凝固 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
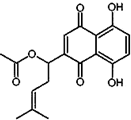 乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法错误的是( )
乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法错误的是( )| A. | 该分子中含有1个手性碳原子 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1mol 乙酰紫草素最多可与2molBr2反应 | |
| D. | 1mol乙酰紫草素最多可与2molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
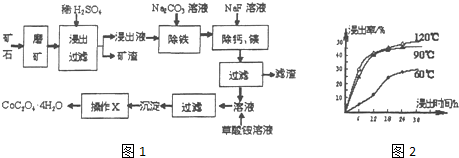
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
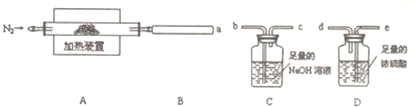
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com