A
分析:A、根据N=
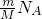
计算含有的分子数,注意只有气体的体积受温度和压强的影响;
B、根据一个气体分子中含有的原子个数判断;
C、常温常压下,气体摩尔体积不是22.4L/mol;
D、根据混合气体的物质的量和分子构成判断.
解答:A、64gSO
2的物质的量是1mol,所以64gSO
2中含有的分子数为N
A,故A正确;
B、同温同压下,相同体积的任何气体单质所含的原子数可能相等也可能不相等,与分子中含有的原子个数有关,有的气体单质的单原子分子,如稀有气体,有的是双原子分子,如氮气、氢气和氧气等,有的是三原子分子,如臭氧分子,故B错误;
C、常温常压下,气体摩尔体积不是22.4L/mol,所以11.2LCl
2含有的分子数不是0.5N
A,故C错误;
D、标况下,22.4LN
2和O
2的混合气体的物质的量是1mol,每个分子中含有的原子都是2个,所以22.4LN
2和O
2的混合气体所含的原子数为2N
A,故D错误;
故选A.
点评:本题考查常用化学计量的有关计算,难度不大,注意只有有关气体体积的计算才与温度和压强有关.

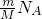 计算含有的分子数,注意只有气体的体积受温度和压强的影响;
计算含有的分子数,注意只有气体的体积受温度和压强的影响;

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案