




 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��п��������ͭƬ�������ݲ��� |
| B��ͭƬ�������� |
| C��������пƬ����������ͭƬ |
| D����������ͭƬ���汻��ԭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A������������ʱ�ƾ�Ũ��Խ�������ǿ��Խ�� |
| B������ʱ����·��������ΪX��Y |
| C����������X������pH���� |
| D������ܷ�ӦΪ2CH3CH2OH+O2��2CH3CHO+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������ڵ�����У�O2���ɸ����������� |
| B����ص��ܷ�Ӧ�ǣ�2C4H10 + 13O2 �� 8CO2 + 10H2O |
| C��ͨ�������һ���Ǹ������缫��ӦΪ��O2 + 4e- = 2O2- |
| D��ͨ�붡���һ�����������缫��ӦΪ��C4H10 + 26e- + 13O2 = 4CO2 + 5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��ȼ�ϵ�ؽ���ѧ��ת��Ϊ���� |
| B��a�Ǽ״���b������ |
| C�����Ӵ�M�缫����������Ĥ����N�缫�� |
| D��������Ӧ��CH4O - 6e- + H2O = CO2��+ 6H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
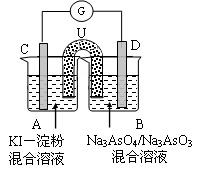

 AsO��3��+I2+H2O����B���м���������Ũ�����ᣬ����G��ָ������ƫ�ơ���ʱA���е���Ҫʵ�������� D�缫�ϵĵ缫��ӦʽΪ
AsO��3��+I2+H2O����B���м���������Ũ�����ᣬ����G��ָ������ƫ�ơ���ʱA���е���Ҫʵ�������� D�缫�ϵĵ缫��ӦʽΪ �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A����˹�����ǹ���ʱ������ڵ�·�е����ɵ缫b����缫a |
| B���缫b��������O2���ɵ缫a����缫b |
| C���缫a�ķ�ӦʽΪ��CH4��4O2����8e��===CO2��2H2O |
| D����������������1 mol O2��ͨ��ʱ������ת��4 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.2 mol�� | B��0.3mol�� |
| C��0.4 mol | D��0.6 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A��a��ͨ������ |
| B��b��Ϊ��������������˻�ԭ��Ӧ |
| C����װ����ֻ�漰������ʽ������ת�� |
| D��P-�Ͱ뵼�����ӵ��ǵ�ظ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com