
为达到相应的实验目的,下列实验的设计或操作最合理的是( )
A. 为测定一定浓度的NaOH溶液放置空气中是否部分转化为Na2CO3,用酚酞作指示剂,用标准盐酸溶液滴定
B. 为观察Mg条在CO2气体中的燃烧,在一个集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部
C. 为比较Cl与S元素的非金属性强弱,相同条件下,测定相同浓度的NaCl溶液和Na2S溶液的pH值
D. 给盛有铜与浓硫酸的试管加热,发现试管底部出现灰白色固体,为检验其中的白色固体为无水硫酸铜,可直接向试管中加入适量水
考点: 化学实验方案的评价.
分析: A.为酸滴定碱,选择酚酞作指示剂,反应终点与指示剂的变色范围接近;
B.应用坩埚钳夹持燃烧,不能投入上述集气瓶底部;
C.比较非金属性强弱,应用最高价含氧酸的酸性进行比较;
D.不能直接向试管中加入适量水,浓硫酸剩余时加水放出大量的热可导致液滴飞溅.
解答: 解:A.为酸滴定碱,选择酚酞作指示剂,反应终点与指示剂的变色范围接近,则测定一定浓度的NaOH溶液放置空气中是否部分转化为Na2CO3,用酚酞作指示剂,用标准盐酸溶液滴定,故A正确;
B.在一个集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持在中低部燃烧,不能投入上述集气瓶底部,否则易导致集气瓶底部受高温炸裂,故B错误;
C.测定相同浓度的NaCl溶液和Na2S溶液的pH值,可比较盐酸与氢硫酸的酸性,但不能比较Cl、S的非金属性,故C错误;
D.不能直接向试管中加入适量水,浓硫酸剩余时加水放出大量的热可导致液滴飞溅,则取反应后的白色固体在烧杯中加水溶解观察是否变为蓝色,故D错误;
故选A.
点评: 本题考查化学实验方案的评价,为高频考点,涉及中和滴定实验、非金属比较、燃烧、盐类水解以及物质检验等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组反应中,硝酸既表现了氧化性,又表现了酸性的是( )
A. C+HNO3 B. SO2+HNO3 C. Fe(OH)3+HNO3 D. FeO+HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
|
| A. | HCl和NaOH反应的中和热△H=﹣57.3 kJ•mol﹣1,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ•mol﹣1 |
|
| B. | CO(g)的燃烧热是283.0 kJ•mol﹣1,则2CO2(g)═2CO(g)+O2(g)反应的△H=(2×283.0)kJ•mol﹣1 |
|
| C. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
|
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用.下列实验中所选用的仪器合理的是( )
①用50mL量筒取5.2mL稀硫酸; ②用分液漏斗分离苯和四氯化碳的混合物;③用托盘天平称量11.7g氯化钠晶体;
④用碱式滴定管取23.10mL溴水; ⑤用瓷坩埚灼烧各种钠的化合物;⑥用250mL容量瓶配制250mL 0.2mol/L的NaOH溶液.
A. ①②④ B. ②③④⑥ C. ③⑥ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
根据如图海水综合利用的工业流程图,判断下列说法正确的是( )已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等
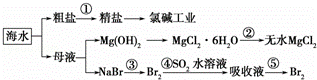
A. 除去粗盐中杂质(Mg2+、SO42﹣、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. 在过程②中将MgCl2•6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
D. 从第③步到第⑤步的目的是为了浓缩
查看答案和解析>>
科目:高中化学 来源: 题型:
8.34g FeSO4•7H2O样品在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示.下列说法中正确的是( )
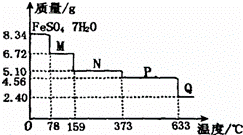
A. 温度为78℃时固体物质M的化学式为FeSO4•5H2O
B. 温度为l59℃时固体物质N的化学式为FeSO4•3H2O
C. 在隔绝空气条件下由N得到P的化学方程式为FeSO4 FeO+SO3↑
FeO+SO3↑
D. 取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
过量的铜与浓硫酸在加热条件下的反应会因硫酸浓度下降而停止.为测定反应残余清液中硫酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量BaCl2溶液反应,称量生成的BaSO4质量.
乙方案:与足量锌反应,测量生成氢气的体积.
回答下列问题:
(1)判定甲方案不可行,理由是 .
(2)甲同学用图1所示装置进行乙方案的实验.
①检查此装置气密性的方法
②使Y形管中的残余清液与锌粒反应的正确操作是将 转移到 中.残余清液与锌粒混合后的现象
③反应完毕,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变.气体体积逐次减小的原因是 (排除仪器和实验操作的影响因素).
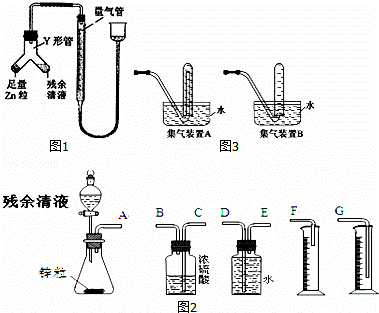
(3)乙同学拟选用图2实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接 接 接 (填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后残余清液就不能顺利滴入锥形瓶.其原因是 .
③乙同学滴入锥形瓶中的残余清液体积为aml,测得量筒中水的体积为bml(假设体系中气体为标准状况),残余清液中硫酸的物质的量浓度的表达式 (用a、b表示)
④某学生想用排水法收集氢气,并检验其纯度,应选择图3集气装置 (填A或B)
查看答案和解析>>
科目:高中化学 来源: 题型:
北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子化合物,具有良好的超导性.下列有关分析正确的是( )
|
| A. | K3C60中只有离子键 | B. | K3C60中不含共价键 |
|
| C. | 该晶体在熔融状态下能导电 | D. | C60与12C互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 石灰水与过量碳酸氢钠溶液反应:HCO |
|
| B. | 向沸水中滴加饱和的FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O |
|
| C. | 氧化铜与稀硫酸反应:2H++O2﹣═H2O |
|
| D. | 碳酸氢钠溶液中加入盐酸:CO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com