
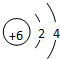 .
.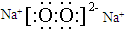 ;如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -.
;如果A、B均由三种元素组成,B为两性不溶物,由A转化为B的离子方程式AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -. 分析 X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y两元素最高正价与最低负价代数和均为0,原子序数均小于O元素,为ⅠA族、ⅣA族元素,故X为H元素、Y为C元素;Q与X同主族,结合原子序数可知,Q为Na元素;
(4)①若上述五种元素中的若干种组成的化合物A、B、C、D,C是溶于水显酸性的气体,C为CO2,D是淡黄色固体,D为Na2O2,
②如果A、B均由三种元素组成,B为两性化合物,且不溶于水,则B为Al(OH)3,A为NaAlO2,A与过量的CO2反应生成生成氢氧化铝沉淀与碳酸氢钠,据此进行解答
解答 解:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素、R为Al;X、Y两元素最高正价与最低负价代数和均为0,原子序数均小于O元素,为ⅠA族、ⅣA族元素,故X为H元素、Y为C元素;Q与X同主族,结合原子序数可知,Q为Na元素,
(1)Y为C元素,Y的原子结构示意图为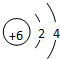 ,
,
故答案为: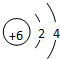 ;
;
(1)同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Na>Al>C>O>H,
故答案为:Na>Al>C>O>H;
(2)QX为NaH,NaH为离子化合物,其电子式为:Na+[:H]-;NaH与水反应生成氢氧化钠和氢气,反应的化学方程式为:NaH+H2O=NaOH+H2↑,
故答案为:Na+[:H]-;NaH+H2O=NaOH+H2↑;
(3)X为H、Z为O,二者形成的两种化合物为水、双氧水,其电子式分别为: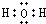 、
、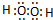 ,
,
故答案为: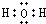 ;
;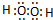 ;
;
(4)由以上某些元素组成的化合物A、B、C、D有如下转化关系A$?_{D}^{C}$B(在水溶液中进行),其中,C是溶于水显酸性的气体,则C为CO2,D是淡黄色固体则D为Na2O2,其电子式为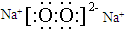 ,如果A、B均由三种元素组成,B为两性不溶物,则B为Al(OH)3,A为NaAlO2,由A转化为B的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
,如果A、B均由三种元素组成,B为两性不溶物,则B为Al(OH)3,A为NaAlO2,由A转化为B的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为: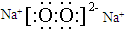 ;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -.
;AlO2-+CO2+2H2O=Al(OH)3↓+HCO3 -.
点评 本题考查了位置、结构与性质关系的应用,题目难度中等,正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期表、元素周期律的关系,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| B. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| C. | 苯酚有一定毒性,不能作消毒剂和防腐剂 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
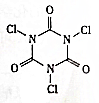 三氯异氰尿酸(结构简式如图)是养蚕业和水产养殖业最重要的消毒剂.三氯异氰尿酸水解生成X和NH4HCO3.下列关于X的说法不正确的是( )
三氯异氰尿酸(结构简式如图)是养蚕业和水产养殖业最重要的消毒剂.三氯异氰尿酸水解生成X和NH4HCO3.下列关于X的说法不正确的是( )| A. | X的结构式为H-Cl-O | B. | X有强氧化性 | ||
| C. | X属于弱酸 | D. | X属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L与0.2 mol/L醋酸溶液,c(H+)之比 | |
| B. | 0.1 mol/L H2S溶液,c(S2-)与c(H+)之比 | |
| C. | pH=10的Ba(OH)2溶液与pH=10的氨水,溶质的物质的量浓度之比 | |
| D. | pH=3的硫酸与pH=3的醋酸溶液,c(SO42-)与c(CH3COO-)之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 称取Na2CO3、NaHCO3固体各2g,分别加入两只大试管中,再各加10mL蒸馏水,充分溶解后各滴入2滴酚酞溶液,观察到如图所示现象.下列说法中正确的是( )
称取Na2CO3、NaHCO3固体各2g,分别加入两只大试管中,再各加10mL蒸馏水,充分溶解后各滴入2滴酚酞溶液,观察到如图所示现象.下列说法中正确的是( )| A. | 试管a溶解过程中温度下降 | |
| B. | 试管b中放入的是NaHCO3固体 | |
| C. | 两试管中水的离子积常数:a<b | |
| D. | 对比液体颜色可知常温下水解程度:CO32->HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
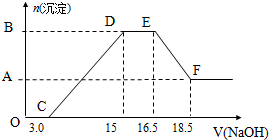 HNO3与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH3的一种或几种.现有一定量的Al粉和Fe粉的混合物与100mL,稀HNO3充分反应,反应过程中无任何气放出.在反应结束后的溶液中,逐渐加入4mol•L-1的NaOH溶液,加入NaOH溶液的体积(mL)与产生沉淀的物质的量关系如图.请回答:
HNO3与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH3的一种或几种.现有一定量的Al粉和Fe粉的混合物与100mL,稀HNO3充分反应,反应过程中无任何气放出.在反应结束后的溶液中,逐渐加入4mol•L-1的NaOH溶液,加入NaOH溶液的体积(mL)与产生沉淀的物质的量关系如图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 位于第七周期第Ⅷ族 | |
| B. | 具有“两性” | |
| C. | 原子核外共有6个电子层 | |
| D. | 该原子中,中子数与质子数之差为43 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
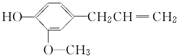 ,丁香酚不具有的性质是( )
,丁香酚不具有的性质是( )| A. | 与金属钠反应 | B. | 与NaOH溶液反应 | ||
| C. | 与碳酸钠反应放出CO2 | D. | 能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| B. | 、SiO2是酸性氧化物,能与NaOH溶液反应 | |
| C. | 、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | .除去石英中的少量碳酸钙,用稀硫酸溶解后过滤分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com