
【题目】乙烯、丙烯都是石油裂解的产物之一,回答下列问题:
(1)乙烯能使溴水褪色,写出其反应的化学方程式;
(2)在一定条件下,丙烯除了与氯化氢、氢气等发生反应外,丙烯分子间还可以发生加聚反应,请写出其反应的化学方程式 , 丙烯发生加聚反应得到的产物(填:“能”“不能”)使酸性KMnO4溶液褪色,丙烯分子中能够共平面的原子最多为个.
【答案】
(1)CH2=CH2+Br2→CH2BrCH2Br
(2)nCH2=CHCH3 ![]()
![]() ;不能;7
;不能;7
【解析】解:(1)乙烯可以和溴水发生加成反应,使溴水褪色,生成1,2﹣二溴乙烷,反应为CH2=CH2+Br2→CH2BrCH2Br,所以答案是:CH2=CH2+Br2→CH2BrCH2Br;(2)丙烯与乙烯互为同系物,丙烯发生加聚反应的方程式是:nCH2=CHCH3 ![]()
![]() ,加聚产物中不再有碳碳双键,所以丙烯发生加聚反应得到的产物不能使酸性KMnO4溶液褪色,丙烯分子中能够共平面的原子最多为7个,即和乙烯结构相同的3个碳原子以及3个氢原子,还有甲基上的一个氢原子,所以答案是:nCH2=CHCH3
,加聚产物中不再有碳碳双键,所以丙烯发生加聚反应得到的产物不能使酸性KMnO4溶液褪色,丙烯分子中能够共平面的原子最多为7个,即和乙烯结构相同的3个碳原子以及3个氢原子,还有甲基上的一个氢原子,所以答案是:nCH2=CHCH3 ![]()
![]() ;不能;7.
;不能;7.


科目:高中化学 来源: 题型:
【题目】【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)写出对应装置中选用的物质:A______________________,B________________,C________________;
(2)其中装置B中所盛试剂的作用为___________________;C中反应的离子方程式为_______________________________。
(3)乙同学的实验原理是________________________________________________;写出B处的离子方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质与常用危险化学品的类别不对应的是( )
A.CH4、汽油——易燃液体B.H2SO4、NaOH——腐蚀品
C.白磷——自燃物品D.红磷 、硫磺——易燃固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和.
(1)A为______,C为______.(填元素符号)
(2)写出A、B的化合物与E反应的化学方程式:______.
(3)A、B两元素形成的化合物属______(填“离子”或“共价”)化合物.
(4)写出D的最高价氧化物的水化物和A单质反应的化学方程式:______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
(1)有科学家提出可利用FeO吸收和利用CO2 , 相关热化学方程式如下:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s)△H=﹣76.0kJmol﹣1
①上述反应中每生成1mol Fe3O4 , 转移电子的物质的量为mol.
②已知:C(s)+2H2O(g)=CO2 (g)+2H2(g)△H=+113.4kJmol﹣1 , 则反应:
3FeO(s)+H2O (g)=Fe3O4 (s)+H2 (g)的△H= .
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2 (g)CH4 (g)+2H2O(g)△H=QkJmol﹣1 , 向一容积为 2L的恒容密闭容器中充人2molCO2和8mol H2 , 在 300℃时发生上述反应,达到平衡时,测得CH4的浓度为0.8molL﹣1 , 则300℃时上述反应的平衡常数K= . 200℃时该反应的平衡常数K=64.8,则该反应的Q(填“>”或“<”)0.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.1000 molL﹣1KOH液滴定未知浓度的醋酸,其操作分解为如下几步: A.移取20mL待测醋酸注入洁净的锥形瓶,并加入2~3滴指示剂
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写);
(2)上述B步骤操作的目的是;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对最终滴定结果的影响是 . (填“增大”、“减小”、或“不变”)
(4)A步骤中,使用的指示剂为 , 判断到达滴定终点的实验现象是:;
(5)如图1为某一次碱式滴定管滴定前液面,其读数值为mL,图2为滴定结束液面,则本次滴定过程共使用了mLKOH标准溶液 
(6)为标定某醋酸溶液的准确浓度,用0.1000molL﹣1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为 . (保留小数点后四位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属单质A,经如下图所示的过程转化为含氧酸D,已知D为常见强酸
![]()
请回答下列问题:
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体
①D的化学式是
②在工业生产中B气体的大量排放被雨水吸收后形成了 而污染了环境
(2)若A在常温下为气体,C是红棕色气体。①A和C的化学式分别是:A ;C
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1﹣苯乙醇具有柔和、愉快而持久的玫瑰香气,广泛用于各种食用香精和烟用香精中.实验室以苯乙酮和硼氢化钠为原料制备1﹣苯乙醇的反应原理(图1)、装置(图2)和有关数据如表:
试剂 | 熔点(℃) | 沸点(℃) | 密度(gcm﹣3) | 溶解性 | ||
水 | 乙醇 | 乙醚 | ||||
1﹣苯乙醇 | 20 | 203.4 | 1.013 | 不溶 | 溶 | 溶 |
苯乙酮 | 19.7 | 202.3 | 1.028 | 不溶 | 溶 | 溶 |
硼氢化钠 | ﹣ | ﹣ | 1.076 | 溶 | 溶 | 不溶 |
乙醚 | ﹣116.3 | 34.6 | 0.713 | 微溶 | 溶 | ﹣ |
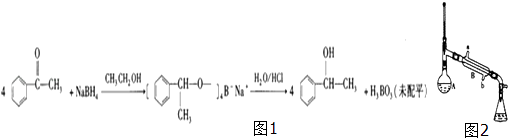
实验步骤:①在烧杯中加入15mL 95%的乙醇和0.1g硼氢化钠,搅拌下,再滴入8mL苯乙酮,控制温
度在48℃~50℃,滴加完毕,室温下放置15min.
②在搅拌的条件下,慢慢滴加6mL 3mol/L的盐酸.
③水浴加热,使反应液中大部分乙醇蒸出,出现分层,再加入10mL乙醚.将混合反应液倒入分液漏
斗,分离上述液体,水层再用10mL乙醚萃取,合并两次分液得到的有机相.
④加入适量无水硫酸镁,静置片刻,过滤除去硫酸镁固体.再加入0.6g无水碳酸钾,然后进行简单蒸
馏除去乙醚.
⑤经减压蒸馏得到1﹣苯乙醇4.5g(减压蒸馏可降低有机物的沸点).
(1)反应中加入乙醇的目的是 .
(2)反应完成后,蒸出大部分乙醇,反应液出现分层,上层为(填“水层”或“有机层”,下同),加入10mL乙醚,充分振荡后,上层为 .
(3)装置中仪器A的名称为 , 在本实验中最好选用的规格是(填“50mL”、“100mL”或“200mL”);仪器B中冷凝水由(填“a”或“b”)口流出.
(4)步骤④中加入无水硫酸镁的作用是 .
(5)步骤④蒸馏除去乙醚时,应采用的最佳加热方式为(填字母序号)a.酒精灯加热 b.水浴加热 c.油浴加热 d.酒精喷灯加热.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com